Проведение - нитрование
Cтраница 1
Проведение нитрования при повышенных емперагурах с особству-ет появлению в продуктах реакции 8-нитроизомеров. [1]
Проведение нитрования требует быстрого отвода тепла, выделяющегося в результате реакции. Как указывалось, тепло выделяется не только вследствие собственно экзотермического характера реакции - но и в результате разбавления серной кислоты водой, образующейся в результате процесса. [2]
Проведение нитрования требует быстрого отвода тепла, выделяющегося в результате реакции. Как указывалось, тепло выделяется не только вследствие собственно экзотермического характера реакции, но и в результате разбавления серной кислоты водой, образующейся в результате процесса. [3]
Для проведения нитрования в промышленности производят 60 - 63 % - ю и 98 - 100 % - ю азотную кислоту. [4]
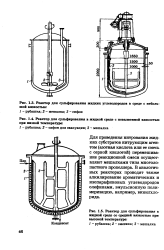
Для проведения нитрования жидких субстратов нитрующим агентом ( азотная кислота или ее смесь с серной кислотой) перемешивание реакционной смеси осуществляют мешалками типа многолопастного пропеллера. В аналогичных реакторах проводят также алкилирование ароматических и изопарафиновых углеводородов олефинами, эмульсионную полимеризацию, например, винилхло-рида. [6]
Необходимость проведения нитрования при высокой температуре вызвана трудностью превращения 4 6-динитрофенол - 2-сульфо-кислоты в тринитропроизводное. [7]
При проведении нитрования м-ксилола в указанных выше условиях, но без катализатора, Холево и Эйтингтон получили те же соединения и с теми же выходами; например, выход моно-нитроксилола из 100 г м-ксилола составлял 35 г, независимо от того, проводилась ли реакция с катализатором или без него. [8]
При проведении нитрования толуола в условиях повышенной против нормы температуры ( от недостатка охлаждения) наблюдалось образование диазо - и даже азосоединепнй от действия на ТОЛУОЛ азотистой кислоты или окиси азота ( ср. [9]
При проведении нитрования м-ксилола в указанных выше условиях, но без катализатора, Холево и Эйтингтон получили те же соединения и с теми же выходами; например, выход моно-нитроксилола из 100 г м-ксилола составлял 35 г, независимо от того, проводилась ли реакция с катализатором или без него. [10]
При проведении нитрования и-ксилола в вышеуказанных условиях, но без катализатора, Холево и Эйтингон получили те же соединения и с теми же выходами; например, выход мононитроксилола из 100 г - ксилола составлял 35 г, независимо от того, проводилась ли реакция с катализатором или без него. [11]
Однако возможно проведение нитрования и посредством избытка водной ( 10 % - ной88 или 20 - 25 % - ной89) азотной кислоты при нагревании. [12]
Однако возможно проведение нитрования и посредством попытка водной ( 10 % - ной чя или 20 - 25 % - ной 89) азотной кислоты при нагревании. [13]
При - проведении нитрования толуола в условиях повышенной против нормы температуры ( от недостатка охлаждения) наблюдалось образование диазо - и даже азосоединений ( от действия азотистой кислоты, соотв. [14]
Однако при проведении нитрования аминов необходимо считаться с наличием в соединении аминогруппы, которая является одним из наиболее мощных электронодонорных заместителей и сильно активирует ароматическое ядро в реакциях электрофильного замещения. Так, аминобензолы подобно фенолам нитруются тетранитрометаноМ в щелочной среде и воспламеняются в контакте с концентрированной азотной кислотой. Для подавления окислительных процессов, сопровождающих нитрование аминобензолов, их предварительно ацилируют или нейтрализуют концентрированной серной кислотой, получая соль. [15]
Страницы: 1 2 3 4