Ванадат
Cтраница 2
 |
Значения Dg и а смеси Ba2 - Ra2 в 4 % - ном ЭДТА на катионообменнике КУ-2. [16] |
Ванадат титана ( 1У) был рекомендован Квереши [19] в качестве высокоселективного неорганического ионообменника для отделения стронция. [17]
Ванадат цезия С52УбС1б, образующийся по реакции ( 9), плавится при 510 С. [18]
Безводный ванадат представляет собой мелкодисперсную кристаллическую массу, так как в процессе удаления воды образуются многочисленные центры новой безводной фазы, количество и развитие которых определяется параметрами процесса обезвоживания. [19]
Ванадаты щелочноземельных металлов получаются прибавлением растворимых солей соответствующих металлов или гидроокисей к растворам ванадатов щелочей. [20]
Ванадаты элементов I - - III групп могут быть использованы при разработке рентгенолюминесцентных экранов. [21]
Ванадаты большинства металлов малорастворимы в воде. Исключение составляют ванадаты калия и натрия. [22]
Ванадат закиси ртути получается в виде белого хлопьевидного осадка при прибавлении избытка нейтрального раствора азотнокислой закиси ртути к нейтральному раствору ванадата. [23]
Ванадаты элементов I-III групп используются для получения люминофоров с белым свечением и со свечением в любом диапазоне видимого света, для применения в ртутных лампах высокого и низкого давления, для цветных и обычных кинескопов. Описаны лазеры на основе орто-ванадатов Y, La, Gd, Lu. В сельском хозяйстве растворимые соли мышьяковистованадиевой кислоты используют в качестве фунгисидов и инсектисидов. Текстильная промышленность применяет ванадаты в качестве протрав при крашении хлопчатобумажных тканей. В медицине применение ванадия основано на окислительных и антисептических свойствах его соединений. Соединения ванадия широко используются в стекольной и керамической промышленности благодаря их разнообразной окраске, а также в фотографии и кинематографии в качестве проявителей, сенсибилизаторов и красителей фильмов и отпечатков. [24]
 |
Зависимость давления перехода шеелит г циркон при 430 от радиуса редкоземельного иона в его ванадатах. [25] |
Как ванадаты, так и арсенаты переходят из цирконовои структуры низкого давления в шеелитовую структуру высокого давления без изменения в первичной координации. Кривые для арсенатов представляют собой аналогичное семейство, но переходы сдвинуты в сторону более низких давлений. Интересен принцип, по которому группируются кривые. Интуитивно можно ожидать, что давление перехода повышается с увеличением ионного радиуса вследствие трудности сжатия более крупных ионов в более плотно упакованную шеелитовую структуру. [26]
Получите ванадаты бария, меди, серебра и свинца взаимодействием растворов солей этих металлов с метаванадатом натрия ( или аммония), употребляя в каждом случае по 3 - 4 капли соответствующих реактивов. [27]
Количество ванадата, образовавшегося при электрохимическом окислении, устанавливают затем титрованием рабочим раствором сульфата железа ( И) в присутствии индикатора фенилантраниловой кислоты; 96500 Кл эквивалентны 1000 мл 1 М раствора сульфата железа ( П), а 1 Кл соответствует 0 104 мл 0 1 М раствора. [28]
Большинство ванадатов окрашены, многие мало растворимы - в воде. Вана-даты можно получить также сплавлением - стехиометрической смеси У2Об с оксидами или карбонатами щелочных металлов. [29]
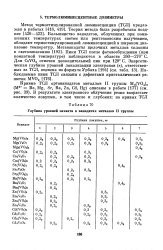 |
Глубина уровней захвата в ванадатах металлов II группы. [30] |
Страницы: 1 2 3 4