Проникновение - молекула - растворитель
Cтраница 3
При осмосе раствор становится более разбавленным, но концентрация молекул растворителя в растворе продолжает оставаться меньшей, чем в растворителе. Однако дополнительное гидростатическое давление, испытываемое молекулами растворителя во внутреннем сосуде и определяемое разностью уровней в обоих сосудах ( h), обусловливает равную скорость прямого и обратного проникновения молекул растворителя через полупроницаемую перегородку. [31]
 |
Схема проникновения молекул воды через полупроницаемую перегородку. [32] |
При осмосе раствор становится более разбавленным, но концентрация молекул растворителя в растворе продолжает оставаться меньшей, чем в растворителе. Однако дополнительное гидростатическое давление, испытываемое молекулами растворителя во внутреннем сосуде и определяемое разностью уровней в обоих сосудах ( / г), обусловливает равную скорость прямого и обратного проникновения молекул растворителя через полупроницаемую перегородку. [33]
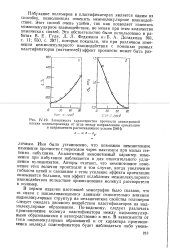 |
Зависимость характеристик прочности анизотропной. [34] |
Ими было установлено, что возможно немонотонное изменение прочности с переходом через максимум при малых степенях набухания. Аналогичный немонотонный характер изменения при набухании наблюдается и для относительного удлинения вулканизатов. Авторы считают, что немонотонное изменение этих величин происходит в том случае, когда увеличение гибкости цепей и связанное с этим усиление эффекта ориентации оказывается большим, чем эффект ослабления межмолекулярного взаимодействия вследствие проникновения молекул растворителя в полимер. [35]
Они мало экранируют электроды, но и не обладают никакой задерживающей способностью. Другую группу составляют пористые сепараторы с радиусами пор от 2 им до 100 мкм. Их применяют в электролизерах и ХИТ. Особую группу сепараторов составляют набухающие мембраны - полимерные материалы, взаимодействующие с водными или неводными растворами. В результате проникновения молекул растворителя в полимерную структуру расстояние между отдельными макромолекулами увеличивается ( мембрана набухает), что создает возможность для миграции имеющихся в растворе ионов. Размер пор в таких мембранах не превышает 2 нм. [36]
 |
Схема осмометра. / - раствор. 2 - вода. [37] |
Если сосуд, переходящий сверху в узкую трубку, не имеющий дна, закрыть снизу полупроницаемой перегородкой и заполнить раствором, то при погружении его в стакан с водой ( рис. 53) в него будет проникать вода из стакана и уровень жидкости в трубке повышается. Это явление называется осмосом. Вода диффундирует через полупроницаемую пленку из мест большей ее концентрации в места меньшей концентрации. В сосуде с раствором создается давление, под действием которого поднимается жидкость в трубке до тех пор, пока не установится равновесие. Осмотическим давлением называется то давление, которое приходится преодолевать приложением к раствору внешнего давления, чтобы задержать молекулы растворителя от проникновения их в раствор через полупроницаемую перегородку. Таким образом, измерив высоту столба жидкости в осмометре h и определив ее плотность, можно найти осмотическое давление я как давление, равное давлению столба жидкости, препятствующему дальнейшему проникновению молекул растворителя в раствор. [38]
Наряду с указанными выше причинами решающее значение для сорбции антибиотиков играет возможность синтеза сильно набухающих ионитов, обладающих большой внутримолекулярной пористостью. Синтетические ионообменные смолы представляют собой трехмерные полимеры. Образование такого рода соединений состоит из стадии синтеза линейных полимеров и их сшивания с возникновением трехмерной макромолекулы. Введение определенного количества сшивающего агента ( например, формальдегида при поликонденсации или дивинилбензола при полимеризации) приводит к образованию полимеров с определенной степенью пористострт, которая проявляется при погружении сорбента в воду или иной растворитель в виде эффекта набухания. Набухание ионообменных смол связано с наличием в молекуле полимера кислотно-основных и других гидрофильных групп. Гидрофильные свойства подобных соединений приводят к сольватации растворителя в результате проникновения молекул растворителя внутрь зерен смолы. Большое количество кислотных или основных функциональных групп, находящихся в ионите, вызывает их значительное набухание в водных растворах, результатом которого является большая внутримолекулярная пористость. Карбоксильные катиониты, например, обладающие большой емкостью, характеризуются и большими значениями коэффициентов набухания, а следовательно, и значительной пористостью. [39]
Страницы: 1 2 3