Пропорциональность - скорость - реакция
Cтраница 1
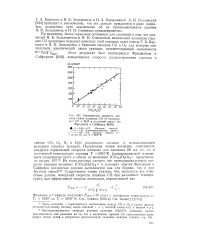 |
Зависимость скорости пла мени окиси углерода СО от содержания СО и Н2О в исходной смеси ( по Фридману и Сайферсу. [1] |
Пропорциональность скорости реакции величине ( НаО) 1, очевидно, нужно рассматривать как указание на то, что в механизме горения СО существенную роль играет обрыв цепей в результате рекомбинаций активных центров ( сравни стр. [2]
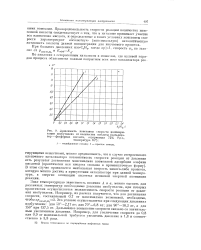 |
Зависимость константы скорости полимери. [3] |
Пропорциональность скорости реакции количеству нанесенной кислоты свидетельствует о том, что в катализе принимает участие вся нанесенная кислота, и определенные в таких условиях константы скорости характеризуют абсолютную ( максимальную) каталитическую активность кислоты данной концентрации для изучаемого процесса. [4]
Пропорциональность скорости реакции разным количествам наносимого вещества свидетельствует об отсутствии диффузионных осложнений. [5]
Пропорциональность скорости реакции экспоненциальному сомножителю ехр - А / Т была установлена Дж. [6]
Пропорциональность скорости реакции концентрации превращающегося вещества представлялась, однако, не согласующейся с ТАС: появление молекул с энергией, большей по сравнению со средней, происходит в результате энергообмена при соударениях частиц, т.е. скорость реакции должна быть пропорциональна квадрату их концентрации. Перрен в 1919 г. предложил радиационную теорию активации частиц при поглощении ими ПК-излучения стенок сосуда. Ее несостоятельность была вскоре показана Ленгмюром. [7]
Из пропорциональности скоростей реакций ( е) - ( б) концентрации партнеров по соударениям и из сравнения абсолютных величин и температурных зависимостей констант скоростей этих реакций и реакций ( а) - ( d)) следует, что при достаточно низких плотностях реакции рекомбинации идут с гораздо меньшими скоростями, чем бимолекулярные реакции. [8]
Поэтому пропорциональность скорости реакции ее сродству достаточно далеко от равновесия ( как это наблюдалось, например в работе [407] для гидрирования бензола на никель-цинк-хромовом катализаторе) скорее указывает на специфику стадийного механизма и кинетики процесса, чем на выполнение линейного закона по термодинамическим причинам. [9]
Наблюдаемая на опыте пропорциональность скорости реакции квадратному корню из концентрации кислорода и в этом случае является веским доводом в пользу теоретического механизма реакции, активную роль в котором играют атомы О. [10]
В работе [12] было показано, что пропорциональность скорости реакции первой степени концентрации амальгамы для концентрированных амальгам означает пропорциональность скорости реакции корню квадратному из активности амальгамы. [11]
Вследствие участия в бензидиновой перегруппировке двух протонов наблюдается пропорциональность скорости реакции квадрату концентрации кислоты. [12]
Первое предположение о гетерогенно-каталитической реакции должно приводить к пропорциональности скорости реакции поверхности сосуда. Уже поэтому мы можем сделать вывод, что реакция распада в свежих сосудах по крайней мере в ряде случаев не является простой гетерогенной каталитической реакцией. [13]
При добавках перекиси бен-зоила с самого начала реакции наблюдается пропорциональность скорости реакции корню квадратному из концентрации перекиси бензоила. [14]
Заменяя 6А выражением изотермы Лэнгмюра, мы, в предельных случаях, получаем либо пропорциональность скорости реакции первой степени объемной концентрации вещества А, либо независимость скорости реакции от объемной концентрации вещества А. [15]
Страницы: 1 2 3