Пропорциональность - скорость - реакция
Cтраница 2
В работе [12] было показано, что пропорциональность скорости реакции первой степени концентрации амальгамы для концентрированных амальгам означает пропорциональность скорости реакции корню квадратному из активности амальгамы. [16]
Однако механизм инициирования реакционных цепей гидроперекисями при термическом автокаталитическом окислении гораздо сложнее, чем рассмотренный выше, на что указывает пропорциональность скорости реакции первой степени концентрации гидроперекиси. Раньше считали, что небольшие, но конечные скорости окисления, которые, по-видимому, имеют место при отсутствии гидроперекиси ( см. рис. 52), связаны с процессами инициирования, в которых не принимают участия перекиси. [17]
Общей чертой топохимических процессов, не лимитирующихся диффузией, является их автокаталитический характер и прохождение скорости процесса через максимум, а также пропорциональность скорости реакции текущей величине поверхности раздела исходной и конечной твердых фаз. [18]
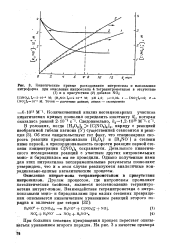 |
Кинетические кривые расходования нитроксила и накопления нитроформа при окислении нитроксила 4 тетранитрометаном в отсутствие. [19] |
Об этом свидетельствует тот факт, что стационарная скорость реакции пропорциональна [ Н202 ] и [ RaNO ] в степени ниже первой, а пропорциональность скорости реакции первой степени концентрации C ( N02) 4 сохраняется. [20]
Японские ученые считают, что полимеризация а-метилстиро ла, инициированная у-излучением, протекает по радикальному механизму и приводят в доказательство этому следующие данные: 1) нафталин и нитробензол ингибируют реакцию; 2) при 20 С реакция может быть вызвана фотохимически или окислительно-восстановительными инициаторами; 3) если мономер высушить над Na, то величина G составляет 1000; 4) пропорциональность скорости реакции мощности дозы в 1 - й степени можно объяснить, если учесть реакцию передачи, приводящую к обрыву цепей. [21]
Пропорциональность скорости реакции количеству наносимого вещества свидетельствует об отсутствии диффузионного торможения. [22]
Бутилгидроперекись расходуется в процессе синтеза в соответствии с кинетическим уравнением реакции второго порядка. Это отвечает пропорциональности скорости реакции концентрациям гидроперекиси и изоолефина в первой степени. Стадия образования карбоний-иона из олефина и кислоты по реакции ( 1) в нашей системе проходит сравнительно быстро и успевает достигнуть равновесия. [23]
В работах Пневой с Борисовой [6] и Пневой с Селютиной [7], осуществлявших окисление изопропилового спирта при повышенных температурах ( 115) и давлении 2 5 атм, методом инициирующих добавок были получены данные, доказывающие цепной, вы-рожденно-разветвленный механизм реакции окисления изопропилового спирта с квадратичным обрывом цепей. Об этом свидетельствовала полученная авторами пропорциональность скорости реакции корню квадратному из скорости инициирования. [24]
В работах Пневой с Борисовой [6] и Пневой с Селютиной [7], осуществлявших окисление изопропилового спирта при повышенных температурах ( 115) и давлении 2 5 атм, методом инициирующих добавок были получены данные, доказывающие цепной, вы-рождепно-разветвленный механизм реакции окисления изопропилового спирта с квадратичным обрывом цепей. Об этом свидетельствовала полученная авторами пропорциональность скорости реакции корню квадратному из скорости инициирования. [25]
Хотя уравнению изотермы Лзнгмюра (III.6) вряд ли точно под - чиняются многие системы, оно оказывается весьма полезным при определении формально-кинетического порядка каталитических реакций. Принципом, лежащим в основе метода определения порядка каталитических реакций, является пропорциональность скорости реакции значениям 9 адсорбированных частиц или выполнение закона действующих поверхностей. [26]
&; - константа равновесия кетон - енол. Единственный вывод, который JVIOJKHO сделать из данных, относящихся к высокой кислотности, заключается в пропорциональности скорости реакции произведению концентраций иода и кетонной формы. Это может соответствовать реакции через енольную форму [ уравнение ( 127) ], но равным образом и непосредственной реакции второго порядка между иодом и кетоном без превращения в енол. Следовательно, данные по иодированию в сильнокислой с реде не дают оснований для выбора между двумя механизмами Однако постепенный переход от несомненно двухстадий-ного механизма иодирования через енольную форму при низких кислотностях к тем закономерностям, которые наблюдаются в сильнокислой среде, дает веские основания считать, что в сильнокислой среде реализуется тот же самый механизм. [27]
В настоящее время принято считать, что даже мономолекулярные реакции для своего осуществления требуют столкновений, посредством которых молекулы получают необходимую энергию активации. По существу различие между моно - и бимолекулярными реакциями состоит в том, что в то время как при бимолекулярной реакции за эффективным столкновением непосредственно следует реакция, при мономолекулярной реакции между столкновением и превращением молекул протекает определенный промежуток времени, в течение которого энергия, повидимому, перераспределяется по различным степеням свободы. Пропорциональность скорости реакции первой степени концентрации, а не ее квадрату, объясняется тем, что молекула может дезактивироваться благодаря столкновению с другой молекулой в течение этого промежутка времени. При низких давлениях, когда средний промежуток времени между столкновениями становится больше промежутка времени между активацией и превращением, процесс должен стать в кинетическом смысле бимолекулярным. Это действительно наблюдалось для большого числа так называемых газовых мономолекулярных реакций ( Успехи физической химии, гл. [28]
Следует подчеркнуть, что вид зависимости скорости реакции от условий эксперимента совершенно необычен. Отсутствует даже привычная пропорциональность скорости реакции навеске твердого реагента. Этот факт, наряду со своеобразной зависимостью скорости реакции от скорости потока газа может создать ложное впечатление о влиянии диффузионного торможения на наблюдаемую кинетику реакции. Заметим также, что зависимость макс от k и pj отнюдь не линейна. [29]
 |
Кинетические кривые накопления радикалов при 300 К. [30] |
Страницы: 1 2 3