Nh-протон
Cтраница 2
При растворении диэтиламина в растворителе, способном к образованию водородных связей с протоном группы NH ( например, в простых эфирах), химический сдвиг NH-протона диэтиламина будет заметно изменяться с изменением концентрации. [16]
Данные спектра ПМР 60 МГц красителя в ДМСО-О6 указывают на одну Et-группу типа СНзСН2ОСО - и около 14 Н в ароматической области, которая может включать NH-протон. Синглет 10 2 согласуется с ОН или NH. [17]
Однако резонанс от протонов группы СН для транс - [ Соеп2С12 ] проявляется в виде квинтета, получающегося вследствие спин-спинового взаимодействия типа А2А2Х2Х2 между СН - и NH-протонами. Как указано выше, резонанс NH-протонов проявляется в виде широкой полосы. [18]
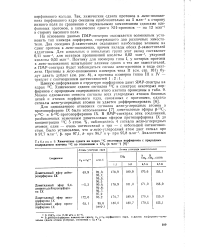 |
Химические сдвиги на ядрах 3С некоторых порфиринов с природным содержанием изотопа 13С по отношению к CS2 ( в млн-1. [19] |
Так, химические сдвиги протонов в жезо-положе - Н иях порфинового ядра смещены приблизительно а 5 млн-1 в сторону низкого поля по сравнению с нормальными химическими сдвигами оле-финовых протонов, а химические сдвиги NH-протонов - а 12 мля 1 в сторону высокого поля. [20]
Однако резонанс от протонов группы СН для транс - [ Соеп2С12 ] проявляется в виде квинтета, получающегося вследствие спин-спинового взаимодействия типа А2А2Х2Х2 между СН - и NH-протонами. Как указано выше, резонанс NH-протонов проявляется в виде широкой полосы. [21]
Значительно более полезными являются сигналы NH-протонов пар оснований, участвующих в образования двуспиральных участков по Уотсону - Крику. [22]
Обычно в области резонанса NH проявляются по крайней мере три полосы. В каждой этилендиаминовой группировке имеются четыре различно ориентированных NH-протона. [23]
В табл. 4.4 приведено положение простых сигналов типичных протонов. Как видно из табл. 4.4, особенно сильное дез-экранирование наблюдается у NH-протонов, находящихся по соседству с кетогруппой и одновременно с бензольным ядром, у С - Н - протонов альдегидной группы, независимо от того, связана она с алкилом или бензольным ядром. Максимальное дезэкранирование протона происходит у сульфогруп-пы вследствие сдвига электронной плотности с - О - Н - связи на атом серы, несущий высокий положительный заряд. Аналогичная причина наблюдается и у альдегидов. Сдвиг сигнала протона в сильное поле у металлоорганических соединений также обусловлен накоплением отрицательного заряда на метилрадикалах. [24]
Сигнал ароматических протонов N-концевой группы при 2 71 является хорошим эталоном для отсчета химических сдвигов. В спектрах олигомеров с п вплоть до 6 четко различимы сигналы NH-протонов от всех остатков; при п6 отдельные сигналы внутренних NH-rpynn начинают перекрываться. [25]
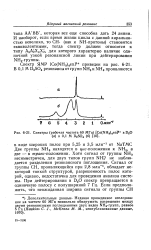 |
Спектры ( рабочая частота 60 МГц [ Co ( NH3 4en ] 3 в D2O ( а и 0 1 М D2SO4 ( б. [26] |
АА ВВ, которая все еще способна дать 24 линии. И наоборот, если время жизни цикла с данной хирально-стью невелико, то СН - ( как и NH-протоны) становятся эквивалентными, тогда спектр должен относится к типу А2А2Х2Х2, для которого характерно наличие одиночной узкой резонансной линии при дейтерировании МН2 - группы. [27]
Как правило, сдвиг сигналов NH-протонов в мочевинных связях больше, чем в уретановых, и составляет 1 05 - 2 03 мд. Комплексообразование LiCl с аллофа-натами и биуретами, образующими внутримолекулярные водородные связи, значительно слабее, и сдвиг сигналов NH-протонов в этих связях существенно меньше. [28]
Реакции нуклеофильного замещения в гетероароматическом ряду могут быть подвержены бифункциональному катализу. Смысл такого катализа ясен из структуры ( 27), где пиридон-2 активирует субстрат к нуклеофильной атаке путем связывания азагруппы и одновременно способствует элиминированию из переходного комплекса NH-протона нуклеофила за счет группы С О. [29]
Они плавятся и возгоняются с разложением; растворимы в углеводородах и в эфире, легко летучи. При исследовании природы связи в этих комплексах обнаружены явления прототропной таутомерии и образование межмолекулярных N - - H... N-связей, обусловленные миграцией NH-протона. [30]
Страницы: 1 2 3 4