Nh-протон
Cтраница 3
Эти авторы считают, что близлежащие и периферические протоны соответственно разэкраниро-ваны и экранированы атомом X. Кроме того, поскольку окружение Нв аналогично окружению NH-протонов в транс-изомере, они отнесли Нв к резонансной линии, имеющей химический сдвиг, аналогичный сдвигу NH-протонов в транс-комплексе. В области, где наблюдаются четыре резонансные линии от группы NH, полосу в самом высоком поле они отнесли к HD, поскольку этот протон является периферическим по отношению к обоим ли-гандам X и связан с атомом азота, находящимся в транс-положении к X. Следующая резонансная линия была отнесена к Нс, который находится у того же атома азота, что и HD, но является близлежащим к одному Х - лиганду. Оставшаяся резонансная линия отнесена к НА. [31]
Ароматические амины, не активированные присутствием полярных группировок в кольце, обычно относятся к этой группе медленно обменивающихся аминов. В промежуточных случаях, наряду с более или менее значительным уширением сигнала NH-протонов, наблюдается отсутствие спин-спиновой связи этих протонов с протонами у а-угле-родного атома. [32]
При растворении диэтиламина в растворителе, способном к образованию водородных связей с протоном группы NH ( например, в простых эфирах), химический сдвиг NH-протона диэтиламина будет заметно изменяться с изменением концентрации. В случае протонов этильных групп подобного изменения наблюдаться не будет, и их будет легко отличить от NH-протонов. [33]
Эти авторы считают, что близлежащие и периферические протоны соответственно разэкраниро-ваны и экранированы атомом X. Кроме того, поскольку окружение Нв аналогично окружению NH-протонов в транс-изомере, они отнесли Нв к резонансной линии, имеющей химический сдвиг, аналогичный сдвигу NH-протонов в транс-комплексе. В области, где наблюдаются четыре резонансные линии от группы NH, полосу в самом высоком поле они отнесли к HD, поскольку этот протон является периферическим по отношению к обоим ли-гандам X и связан с атомом азота, находящимся в транс-положении к X. Следующая резонансная линия была отнесена к Нс, который находится у того же атома азота, что и HD, но является близлежащим к одному Х - лиганду. Оставшаяся резонансная линия отнесена к НА. [34]
Из конформа-ционного анализа следует, что каждая хиральная форма складчатого этилендиаминового кольца имеет набор различных конформаций с очень небольшим или равным нулю энергетическим барьером между ними. Даже если барьер достаточно высок для медленных конформационных превращений, спектр ЯМР вследствие гибкости кольца, по существу, все же является спектром, усредненным по времени. Тем не менее эта усредненная по времени конформация относится, вероятно, к симметрично скошенному типу, в котором имеются две эквивалентные пары СН-протонов, находящиеся в аксиальном и экваториальном положениях к кольцу, а также две эквивалентные пары NH-протонов, которые также подразделяют на аксиальные и экваториальные. Ожидалось, что спектр высокого разрешения может обладать чрезвычайно сложной мультиплетной структурой, но, если линии будут располагаться достаточно близко, они сольются в широкую огибающую полосу, у которой почти или совсем не будет наблюдаться тонкая структура. [35]
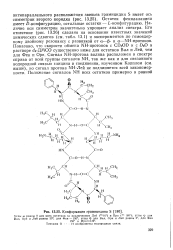 |
Конформация грамицидина S. [36] |
Остаток фенилаланина имеет D-конфигурацию, остальные остатки - L-конфигурацию. Наличие оси симметрии значительно упрощает анализ спектра. Его отнесение ( рис. 13.26) сделано на основании известных значений химических сдвигов ( см. табл. 13.1) и экспериментов по гомоядер-ному двойному резонансу с развязкой от а - - и а - МН-протонов. Показано, что скорости обмена NH-протонов с CD OD и с D2O в растворе de - ДМСО существенно ниже для остатков Вал и Лей, чем для Фен и Орн. Сигнал NH-протона валина расположен в спектре справа от всей группы сигналов NH, так же как и для связанного водородной связью глицина в соединении, изученном Копплом ( см. выше), но сигнал протона NH-Лей не подчиняется всей закономерности. [37]
Наиболее известным методом искажения порфиринового цикла является введение в его периферию заместителей в соседние мезо - и р-положения. Конденсацией 3 4-диал-килпирролов и 2-гидроксиметил - 3 4-диалкилпирролов с бензальдегидами нами синтезирован ряд лезо-фенилзаме-щенных порфиринов с последовательным увеличением искажения макроцикла. Установлено, что искажение существенно влияет на физико-химические свойства порфиринов. С увеличением искажения происходит аддитивный батохромный сдвиг всех полос в электронных спектрах поглощения, слабопольный сдвиг сигналов NH-протонов в спектрах ПМР, уменьшается подвижность на сорбентах, повышается комплексообразующая способность и увеличивается основность порфиринов. [38]
Наиболее известным методом искажения порфиринового цикла является введение в его периферию заместителей в соседние мезо - и ( 3-положения. Конденсацией 3 4-диал-килпирролов и 2-гидроксиметил - 3 4-диалкилпирролов с бензальдегидами нами синтезирован ряд лезо-фенилзаме-щенных порфиринов с последовательным увеличением искажения макроцикла. Установлено, что искажение существенно влияет на физико-химические свойства порфиринов. С увеличением искажения происходит аддитивный батохромный сдвиг всех полос в электронных спектрах поглощения, слабопольный сдвиг сигналов NH-протонов в спектрах ПМР, уменьшается подвижность на сорбентах, повышается комплексообразующая способность и увеличивается основность порфиринов. [39]
 |
Химические сдвиги 14N ( 8СНзМОг - значения в млн 1. [40] |
Если 15N - ЯМР-спектры снимают только для образцов, обогащенных изотопом 16N, то резонансные сигналы ядер 14N наблюдаются и для обычных соединений. При этом варьируют частоту осциллятора дополнительного радиочастотного поля и одновременно наблюдают ПМР-спектр. Как только с помощью дополнительного осциллятора достигается резонансная частота ядер 14N, обнаруживается исчезновение тонкой структуры или сужение сигнала NH-протонов. [41]
Остаток фенилаланина имеет D-конфигурацию, остальные остатки - L-конфигурацию. Наличие оси симметрии значительно упрощает анализ спектра. Его отнесение ( рис. 13.26) сделано на основании известных значений химических сдвигов ( см. табл. 13.1) и экспериментов по гомоядер-ному двойному резонансу с развязкой от а - - и а - МН-протонов. Показано, что скорости обмена NH-протонов с CD OD и с D2O в растворе de - ДМСО существенно ниже для остатков Вал и Лей, чем для Фен и Орн. Сигнал NH-протона валина расположен в спектре справа от всей группы сигналов NH, так же как и для связанного водородной связью глицина в соединении, изученном Копплом ( см. выше), но сигнал протона NH-Лей не подчиняется всей закономерности. [42]
 |
Структура хромофора фталоцианина. [43] |
В нем протоны двух пир-рольных - NH-rpynn подверглись внутренней ионизации и протонная материя циркулирует внутри пространства, состоящего из четырех С-N - связей двукратно заряженного аниона фталоцианина. Электроны ионизации ( их два по числу протонов) спарены и могут занять низшую вакантную ( НВМО) молекулярную орбиталь 16-членного хромофора. Внутренняя ионизация чрезвычайно часто наблюдается в хромофорных системах сложных красителей. Ниже будут приведены примеры таких структур. Хромофор многочисленных фталоцианинов, которые образуются путем замещения Н - атомов в бензольных ядрах или замещением NH-протонов на атомы металлов различных групп периодической системы, является уникальным. Его первая полоса поглощения лежит близко к границе видимой и ИК-области ( 700 нм) и характеризуется максимально возможной вероятностью поглощения квантов света. [44]
 |
Спектры протонов в - положении к аминогруппе. [45] |
Страницы: 1 2 3 4