Протекание - электродный процесс
Cтраница 1
Протекание электродного процесса сопровождается изменением концентрации ионов электролита, участвующих в процессах электрохимического окисления или восстановления. Если ионы образуются в ходе электродного процесса, то их концентрация в приповерхностном слое электрода увеличивается, если они расходуются, то - уменьшается. [1]
На протекание электродных процессов влияет адсорбция органических веществ на поверхности электрода, что широко используется на практике прежде всего для регулирования процессов электроосаждения металлов и защиты металлов от коррозии. [2]
На протекание электродных процессов огромное влияние оказывают природа растворителя и материала электрода, причем глубокая физическая сущность этого влияния пока не раскрыта. [3]
 |
Коэффициенты диффузии некоторых основных анионов ( / и катионов ( 2. [4] |
Возможность протекания электродных процессов и их кинетика определяются также концентрацией молекул, подвергшихся электролитической диссоциации. Активность а ионов, участвующих в процессе, как правило, не соответствует их концентрации С в электролите. Это различие определяется соотношением ауа - С, где уа - коэффициент активности. Только при бесконечном разбавлении уа1, т.е. концентрация растворенного вещества равна его активности, когда взаимодействием ионов можно пренебречь. Такие электролиты называются стандартными. [5]
Если при протекании электродного процесса на электроде образуются газообразные продукты, то возникает необходимость анализа выделяющегося газа. Эту операцию проводят в ячейках специальной конструкции, в которых исследуемый электрод находится под колпаком, снабженным системой для сбора газа и отбора пробы. Более совершенная система, хотя и не всегда применимая, включает особую конструкцию для отбора газа. Исследуемый электрод наносят на тефлоно-вую пористую мембрану, через которую газообразные продукты могут отсасываться в камеру спектрометра или другого анализатора. [6]
Показано, что на протекание электродного процесса влияет лишь природа R1 и R2, но не R и R3; при этом, если заместители R1 и R2 являются ароматическими производными, то перенос единственного электрона протекает обратимо. Образующиеся при переносе электрона свободные радикалы димеризуются по атому углерода. [7]
Рассмотрим влияние различных потоков на протекание электродных процессов. [8]
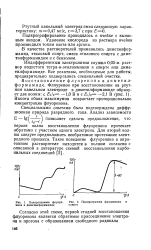 |
Подпрограмма флуоренона в диметалформамиде.| Подпрограмма флуоренона спирте. [9] |
Для второй волны следует предположить необратимое протекание электродного процесса. [10]
Прямая регистрация свободных радикалов при протекании электродных процессов была осуществлена методом ЭПР. [11]
Прямая регистрация свободных радикалов при протекании электродных процессов была осуществлена методом ЭПР. [12]
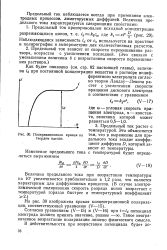 |
Поляризационная кривая на тем, что в выражение для пре-твердом катоде. дельного тока входит коэффи. [13] |
Предельный ток наблюдается всегда при протекании электродных процессов, лимитируемых диффузией. [14]
Перенапряжение всегда вызывается затруднениями при протекании электродного процесса. [15]
Страницы: 1 2 3 4