Протекание - реакция
Cтраница 1
Протекание реакции могут стимулировать различные протонные и льюи-совы кислоты. Во-вторых, стереохими-ческая конфигурация мигрирующей группы сохраняется. [1]
Протекание реакции в этом случае обеспечивается, по-видимому, остаточными ионами натрия. [2]
Протекание реакции зависит от силы электрофила ( кислоты), наличия заместителей, стабилизирующих карбкатион, химической инертности и диэлектрической проницаемости среды. [3]
Протекание реакции ( 56) между изобутанам и растворенными в кислоте углеводородами с образованием алкилата [6] вероятно. [4]
Протекание реакции С3Н8; С3Нв - ( - Н2, сопровождающееся увеличением объема, указывает на окончание процесса дегидрирования. Поэтому понижение давления способствует образованию пропилена при дегидрировании, заканчивающемся реакцией равновесия. [5]
Протекание реакции могут стимулировать различные протонные и льюи-совы кислоты. Во-вторых, стереохими-ческая конфигурация мигрирующей группы сохраняется. [6]
Протекание реакции ( б) подтверждается уменьшением рН раствора, обусловленным выделением в раствор иона водорода при превышении полной емкости. [7]
Протекание реакции возможно лишь на определенном температурном уровне и в определенном интервале температур, которые обеспечиваются подводом или отводом тепла с учетом тепловых эффектов реакций. [8]
Протекание реакций при более низких, чем в газовой фазе, температурах, что дает возможность применять каталитические процессы для термически недостаточно стабильных соединений. [9]
Протекание реакции ( за пределами периода индукции) можно удовлетворительно описать кинетическим уравнением второго порядка, а его константу скорости k в широком диапазоне температур 625 - 2700 К - единым уравнением, соответствующим А ж ж 163 кДж / моль. Скорость расхода ацетилена при пиролизе в различных температурных областях определяется одной основной реакцией, очевидно, димеризации. Эта наиболее медленная стадия сохраняет в широком диапазоне температуры второй порядок и постоянную эффективную А ж 163 кДж / моль. Отклонения от этих закономерностей за период индукции, значительный только при низких температурах, мало сказываются на последующем ходе превращения. Продукты первичного взаимодействия реагируют далее ступенчато и в различных направлениях с образованием более сложных соединений и, в конечном итоге - высокомолекулярных твердых полимеров и сажи. Однако на ходе определяющей стадии расходования исходного ацетилена вторичные явления уже не сказываются. [10]
Протекание реакции по схеме 1 или 2 зависит от строения пирддиниевой соли и условий проведения реакции ( ср. [11]
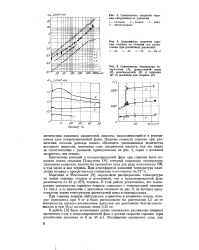 |
Зависимость скорости горения нитраминов от давления.| Зависимость скорости горения тетрила от степени его разложения при различных давлениях.| Зависимость температур по. [12] |
Протекание реакций в конденсированной фазе при горении было показано позже опытами Плясунова [8], который определил температуру плавления вещества, взятого из прогретого слоя для ряда погашенных ВВ, в том числе и для тетрила. [13]
Протекание реакции в кинетической области может быть представлено моделью непрерывного превращения или непроницаемого ядра. Из уравнения ( XV20) следует, что, согласно первой модели, при заданном t степень превращения Хв не зависит от размера частицы; однако это не согласуется с экспериментом. [14]
Протекание реакции по стадийному или слитному механизму зависит от типа реагирующих веществ, природы катализатора, условий окисления и предварительной обработки катализатора, определяющей ещ состав. [15]
Страницы: 1 2 3 4