Протекание - анодная реакция
Cтраница 1
 |
Поляризационные кривые. [1] |
Протекание анодной реакции в значительной мере определяется типом и концентрацией анионов, содержащихся в коррозионной среде. [2]
Протекание анодных реакций в тонких слоях имеет свои специфические особенности. Если обратиться к табл. 19, то легко заметить, что уже при незначительном сдвиге потенциала от стационарного значения, кроме реакций, рассмотренных выше, на аноде могут протекать и реакции электрохимического окисления меди ионами Cl -, SCu2 - и СОз2 - с образованием хлоридов, сульфатов и карбонатов в результате не вторичных процессов, а первичного электрохимического акта. Образующиеся соединения, очевидно, не обладают защитными свойствами. Впрочем, хлориды, сульфаты, карбонаты и гидраты когут образовываться и в результате вторичных реакций за счет взаимодействия перешедших в раствор ионов меди с анионами. Эти соединения, не обладая защитными свойствами, тем не менее оказывают косвенное влияние на процесс наступления пассивного состояния. [3]
Коррозионное растрескивание однофазных сплавов Эделяну связывает с возможностью автокаталитического протекания анодной реакции, приводящего к образованию коррозионных язв, и дальнейшим развитием их в коррозионные трещины. [4]
 |
Зависимость скорости коррозии сплава АМЦ от относительной влажности воздуха при периодическом смачивании 3 % - ным раствором NaCJ. ( 1 раз в сутки. [5] |
Для гомогенных сплавов, скорость коррозии которых определяется в основном скоростью протекания анодной реакции, гораздо большее значение будет иметь уже время пребывания пленки электролита на поверхности металла, которое увеличивается с повышением относительной влажности воздуха. [6]
Первоначальное разблагораживание значений потенциалов авторы связывают с проникновением раствора в поры или трещины в окисной пленке и началом протекания анодной реакции. [7]
Адсорбция ПАВ возможна не только непосредственно на металле анода, но и на кристаллах соли, которые образуются в результате протекания анодной реакции. В этом случае в результате адсорбции ПАВ пассивное состояние электрода наступает быстрее из-за образования такого солевого слоя. Необходимо, однако, заметить, что адсорбция не всегда приводит к торможению анодного процесса. В некоторых случаях возможна активация анодного растворения в результате образования комплексов с ионами растворяемого металла либо вследствие разрушения пассивирующего слоя частицами ПАВ. Такие явления наблюдаются преимущественно при адсорбции неорганических анионов. Аналогичный эффект отмечен А. И. Левиным с сотрудниками в случае анодного растворения металла ( меди) в присутствии органических соединений. Было замечено, что введение высокомолекулярных и коллоидных поверхностно активных веществ влияет также на вязкость раствора. [8]
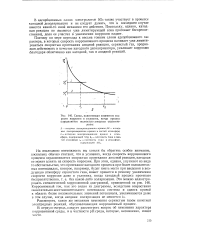 |
Схема, поясняющая изменение скорости коррозии в условиях, когда процесс определяется полностью анодным ограничением. [9] |
Поэтому по мере перехода к весьма тонким слоям адсорбционного характера, в которых скорость коррозионного процесса начинает уже лимитироваться скоростью протекания анодной реакции, сернистый газ, продолжая действовать в качестве катодного деполяризатора, усиливает коррозию благодаря облегчению как катодной, так и анодной реакций. [10]
Если раствор, реагирующий с анодно поляризуемым металлом, содержит компонент, способный катодно восстанавливаться при потенциале, более положительном, чем потенциал протекания анодной реакции, то на поверхности металла одновременно идут обе реакции. Они могут быть локализованы на различных участках поверхности металла, так что часть ее растворяется, а на другой части происходит катодное восстановление. В этом случае, характерном для металлической коррозии, процессы можно геометрически разделить и изучать отдельно. В то же гфемя анодный и катодный процессы могут быть пространственно так сближены, что наблюдать и изучать анодный процесс нельзя отдельно от катодного, если только потенциал не сдвинут в положительную сторону настолько, что катодным процессом можно пренебречь. [11]
Если раствор, реагирующий с анодно поляризуемым металлом, содержит компонент, способный катодно восстанавливаться при потенциале, более положительном, чем потенциал протекания анодной реакции, то на поверхности металла одновременно идут обе реакции. Они могут быть локализованы на различных участках поверхности металла, так что часть ее растворяется, а на другой части происходит катодное восстановление. В этом случае, характерном для металлической коррозии, процессы можно геометрически разделить и изучать отдельно. В то же время анодный и катодный процессы могут быть пространственно так сближены, что наблюдать и изучать анодный процесс нельзя отдельно от катодного, если только потенциал не сдвинут в положительную сторону настолько, что катодным процессом можно пренебречь. [12]
На последнюю возможность мы хотели бы обратить особое внимание, поскольку обычно считают, что в условиях, когда скорость коррозионного процесса ограничивается скоростью протекания анодной реакции, катодная не может влиять на скорость коррозии. [13]
При испытаниях алюминиевых сплавов Ферми и Эванс [48] применяли растворы 0 5 - м, хлористого натрия 0 005 - м, бикарбоната натрия; ускорение процесса при этом испытании достигается за счет влияния бикарбоната натрия как вещества, препятствующего нейтрализации накапливающейся в трещинах кислоты в результате протекания преимущественно анодной реакции. [14]
Ионы Fe2, окисленные бактериями до Fe3, в водных средах образуют гидроксид. Протекание анодных реакций вызывает заметное снижение рН среды, что в свою очередь, наряду с наличием в среде Ог, С02, ионов Fe2, аммонийных солей или нитратов, оптимизирует условия для развития железобактерий. Кроме того, вследствие подкисления среды увеличивается ее электропроводность, что также приводит к возрастанию скорости коррозионного процесса. [15]
Страницы: 1 2