Протекание - анодная реакция
Cтраница 2
Преимущественный контроль скоростью катодной реакции характерен для коррозии металлов в кислых средах, в нейтральных электролитах и атмосферных условиях, а также для коррозии амфотерных металлов в щелочных средах. Контроль скоростью протекания анодной реакции характерен для металлов, способных переходить в пассивное состояние. Смешанный контроль - контроль скоростями обеих реакций - наиболее распространен в практике и встречается в различных условиях, например при коррозии алюминия в нейтральных электролитах. [16]
Отмечается, что коррозионные трещины при развитии в указанных сплавах минуют д-фазу. Коррозионное растрескивание однофазных сплавов связывается с возможностью автокаталитического протекания анодной реакции, приводящей к образованию коррозионных язв с дальнейшим развитием их в коррозионные трещины. [17]
 |
Изменение электродного потенциала вдоль поверхности контактных пар. [18] |
В элементе типа / потенциал изменяется только вдоль поверхности анода, а на катоде потенциал остается постоянным. Это соответствует случаю, когда ток пары определяется скоростью протекания анодной реакции. В элементе типа / / потенциал меняется лишь вдоль поверхности катода, а градиент потенциала вдоль поверхности анода отсутствует. Это соответствует условиям, когда ток элемента определяется скоростью протекания катодной реакции. Этот случай встречается, кстати, очень часто. [19]
Ясно, что этот эффект может проявляться лишь в тех случаях, когда коррозионный процесс в какой-то степени определяется скоростью протекания катодной реакции восстановления кислорода. В условиях же, когда коррозионной процесс определяется скоростью протекания анодной реакции, изменение эффективности работы катода не должно заметно влиять на скорость коррозионного процесса. [21]
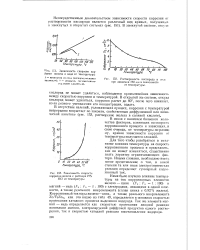 |
Зависимость скорости коррозии железа в воде от темгературы I - замкнутая система ( кислород не может удаляться.. - открытая система ( кислород может удаляться.| Зависимость скорости. [22] |
Коррозионный ток пары железо-цинк, а также реального микроэлемента Zn / FeZn7, как это видно из табл 49, определяется в основном скоростью протекания катодного процесса выделения водорода. Ток же элемента магний - медь определяется как скоростью протекания анодной реакции ионизации магния, контролируемой диффузией продуктов одного растворения, так и скоростью катодной реакции восстановления водорода. [23]
По мере углубления корозионного поражения возрастает концентрация напряжений, к силу чего происходит непрерывное понижение электродного потенциала, увеличивающее разность потенциалов пары и как следствие усиливающее проникновение коррозии в глубь металла. Понижение электродного потенциала н этом случае следует рассматривать как облегчение протекания анодной реакции. Другими словами, повышающаяся концентрация напряжений делает металл на этих участках более химически активным. [24]
Оно показывает, что возрастание сдвига потенциала в положительную сторону от равновесного может только увеличивать скорость процесса. При этом сдвиг потенциала может достигнуть такой величины, при которой возможно протекание других анодных реакций: окисление анионов из раствора или окисление материала электрода с переходом в раствор ионов высшей валентности. [25]
Такая дифференциация поверхности на участки, где преимущественно протекает одна из реакций, приводит к тому, что в системе появляется ток и на поверхности начинают функционировать мощные коррозионные элементы. Этому способствует то обстоятельство, что увеличение скорости анодной реакции на одном из участков и сосредоточение в нем анодного процесса сразу же сильно уменьшает вероятность протекания анодной реакции на других участках. Получается как бы автокаталитический процесс; возникший однажды по тем или иным причинам в одном месте, очаг коррозии стабилизируется в связи с тем, что он электрохимачески защищает остальную часть поверхности. [26]
Такая дифференциация поверхности на участки, где преимущественно протекает одна из реакций, приводит к тому, что в системе появляется ток и на поверхности начинают функционировать мощные коррозионные элементы. Этому способствует то обстоятельство, что увеличение скоро - - сти анодной реакции на одном из участков и сосредоточение в нем анодного процесса сразу же сильно уменьшает вероятность протекания анодной реакции на других участках. Получается как бы автокаталитический процесс; возникший однажды по тем или иным причинам в одном месте, очаг коррозии стабилизируется в связи с тем, что он электрохимически защищает остальную часть поверхности. [27]
В случае нанесения на железо металлов с более положительным потенциалом ( никель, хром, свинец, медь) роль защитного покрытия состоит в создании диффузионного барьера на пути ионов электролита к поверхности железа и изоляции поверхности от газов при химической коррозии. Сплошность гальванического пок рытия является определяющим фактором защиты. При малейшем разрушении покрытия становится возможным протекание анодной реакции покрываемого металла и его растворение по всей поверхности, покрытой электролитом. При этом неповрежденные участки поверхности играют роль катодов. [28]
Страницы: 1 2
