Протекание - ферментативная реакция
Cтраница 2
 |
Скорости реакций сложных эфиров карбобензоксиглицина при 25. [16] |
Скорость определяющей стадией является конформационное изменение фермента. Если для протекания ферментативной реакции необходимо конформационное изменение фермента, индуцируемое субстратом, то маловероятно, чтобы эта стадия в случае различных субстратов протекала с одинаковой скоростью, тем не менее скорости могут быть близкими ( гл. [17]
Кроме фермента и субстрата, для протекания ферментативной реакции часто необходимо также присутствие других веществ. Выше уже описывался решающий опыт, при помощи которого было установлено, что спиртовое брожение нуждается, кроме нетермостойкого, недиализирующегося фермента, еще и в присутствии термостойкого, диализирующегося кофермента. Впоследствии коферменты спиртового брожения ( кокарбоксилаза и кодеги-драза I) удалось выделить; аналогично были выделены коферменты других ферментативных процессов; строение этих коферментов было установлено расщеплением и синтезом. [18]
Скорость биосинтеза жирных кислот лимитируется стадией карбоксилиро вания ацетил - СоА, катализируемого ацетил - СоА - - карбоксилазой. Следовательно, цитрат стимулирует ( увеличивает Fmax) протекание ферментативной реакции, являющейся лимитирующим этапом биосинтеза жирных кислот. Кроме того, поскольку цитрат прочнее связывается с нитевидной ( активной) формой фермента, присутствие цитрата сдвигает равновесие между двумя формами в сторону активной формы. Наоборот, пальмитоил - СоА ( конечный продукт биосинтеза жирных кислот) сдвигает равновесие в сторону неактивной формы. Поэтому по мере образования конечного продукта биосинтеза жирных кислот скорость биосинтеза снижается. [19]
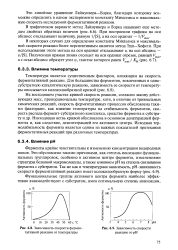 |
Зависимость скорости ферментативной реакции от температуры.| Зависимость скорости реакции от рН. [20] |
На восходящем участке кривой скорость реакции, согласно закону действующих масс, пропорциональна температуре, хотя, в отличие от тривиальных химических реакций, скорость ферментативных процессов обусловлена такими факторами, как влияние температуры на стабильность ферментов, скорость распада фермент-субстратного комплекса, сродство фермента к субстрату и др. Нисходящая ветвь кривой обусловлена в основном денатурацией фермента и, как следствие, дезинтеграцией его активного центра. Исходная термолабильность фермента является одним из важных показателей протекания ферментативных реакций при различных температурах. [21]
Ограничение круга рассматриваемых реакций процессами, протекающими по типу расщепления связи ацил - X, объясняется тем, что только такой тип расщепления связей имеет биохимическое значение. R - COO - p - R), случаи протекания ферментативных реакций гидролиза или переноса ацильной группы по аналогичному механизму не известны. Реакции, катализируемые гидролитическими ферментами, которые наиболее изучены из ацилтрансфераз, обычно протекают по механизму двойного замещения, в результате которого образуется промежуточный ацилфермент ( см. гл. [22]
АТР, белок сорбируется не только на интактной молекуле АТР, но также и на продуктах ее расщепления. Этот тип аффинной хроматографии на иммобилизованном субстрате в условиях, благоприятных для протекания ферментативной реакции, назван динамической аффинной хроматографией. Высказано также предположение, что связывание ферментов в этих условиях определяется скорее константой типа константы Ми-хаэлиса, а не константой ассоциации фермента с интактным субстратом. Динамические аффинные колонки, содержащие иммобилизованные субстраты, могут быть безусловно полезными для обнаружения изменений в связывающих участках активных центров ферментов и для разделения и выделения различных изофермен-тов. [23]
Изучение кинетики и механизма инактивации ферментов составляет одну из задач биокинетики. Выше рассмотрены закономерности инактивации ферментов, в которых концентрация субстрата постоянна, не является переменной величиной. Однако в большинстве случаев в процессе протекания ферментативной реакции в закрытых системах весьма существенное влияние на динамику реакции оказывает истощение системы по субстрату. [24]
В три пробирки наливают по 3 мл панкреатина. Во все пробирки добавляют по 100 мг окрашенного фибрина и инкубируют 30 мин при 37 С. Помечают пробирку, в которой созданы условия для протекания ферментативной реакции, регистрируемой по отщеплению краски от белка. [25]
Низкая температура, а также присутствие в умеренных концентрациях солей или органических растворителей замедляет рост микроорганизмов. Антисептические препараты следует применять с осторожностью, чтобы не вызвать инактивирования. Антибиотики, подобные пенициллину, применяются в тех случаях, когда доказано, что их добавление не препятствует протеканию ферментативных реакций. Одним из наиболее ценных антисептиков оказался толуол, поскольку он не влияет на большинство ферментативных процессов или химических реакций. Для насыщения раствора следует применять достаточное количество толуола; это лучше всего достигается путем подвешивания в замкнутом сосуде, предназначаемом для хранения препарата, небольшой пробирки с несколькими каплями толуола. [26]
 |
График Лайнуивера-Бэрка для идентификации различных типов ингибирования. а - конкурентное ингибирование. б - неконкурентное ингибирование. [27] |
Чаще всего в качестве активаторов выступают ионы металлов, такие, как железо, медь, кобальт, магний и др. Следует различать металлы, находящиеся в составе металлоферментов, так называемые кофакторы, и выступающие в качестве активаторов ферментов. Кофакторы могут прочно связываться с белковой частью фермента, что же касается активаторов, то они легко отделяются от апофермента. Кофакторы являются обязательными участниками каталитического акта; в их отсутствие фермент неактивен. Активаторы усиливают каталитическое действие, но их отсутствие не препятствует протеканию ферментативной реакции. Как правило, металл-кофактор взаимодействует с отрицательно заряженными группировками субстрата. [28]
Анодом в электрохимической реакции служит платиновая пластина, покрытая мембраной типа коллаген - фермент; катод выполнен в виде коробки, изготовленной из угля и пластмассы. Одна сторона угольной пластины ( 4 х 4 х 0 6 см) погружена в электролит, другая - находится на воздухе. Раствор в анодной части ячейки представляет собой 0 1 М фосфатный буфер ( рН 7 7), содержащий субстрат ( молочную кислоту), NAD и электроактивное вещество, например FMN. Фермент добавляют в анодную часть ячейки, а платиновую пластинку используют как анод. Анодная и катодная часть ячейки соединяются солевым мостиком с агар-агаром. Когда электрическая цепь разомкнута, потенциал анода становится более отрицательным вследствие протекания ферментативной реакции в растворе, заполняющем анодную часть ячейки. Равновесие в этом растворе устанавливается только через 30 мин после начала ферментативной реакции. По истечении этого времени цепь замыкают и измеряют ток. Для LDH-коллагеновой мембраны активность фермента определяют в растворе, содержащем 12 5 ммоль молочной кислоты и 1 ммоль NAD в 1 л, причем установлено, что активность фермента остается постоянной в течение более чем 8 измерений. [29]
Страницы: 1 2