Протекание - данная реакция
Cтраница 1
Протекание данной реакции с диолами, а не со спиртами R OH обусловлено более благоприятным значением AS для реакции диолов, чем для спиртов, так как в последнем случае число молекул при переходе от исходных соединений к продукту реакции уменьшается. Альдегиды и кетоны, которые трудно превратить в ацетали, часто образуют их с помощью ортоэфиров, например триэтоксиметана ( этилортоформиат) HC ( OEt) 3 в присутствии NH4C1 в качестве катализатора. [1]
Протеканию данной реакции, вероятно, способствует низкая растворимость амидного соединения ртути. [2]
Протеканию данной реакции иешают альдегиды, кетоны и фенолы, поэтому используют экстракцию аыина хлороформом или эфиром ив щелочного раствора. [3]
Для протекания данной реакции необходим еще один компонент - восстановитель. В технологии СПС ( 1 - 5) в качестве восстановителя используется полигликоль. Реакция получения Сг 3 осуществляется предварительно до введения сшивателя в раствор полимера. [4]
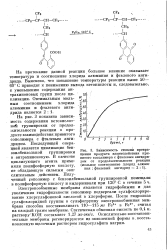 |
Зависимость степени превра. [5] |
На протекание данной реакции большое влияние оказывает температура и соотношение хлорида алюминия и фталевого ангидрида. Выяснено, что повышение температуры реакции выше 50 - 60 С приводит к понижению выхода кетокислоты и, следовательно, к уменьшению содержания ан-трахиноновых групп после циклизации. [6]
Если условия протекания данной реакции таковы, что концентрации всех реагирующих веществ остаются постоянными или почти постоянными, то реакция протекает по нулевому или псевдонулевому порядку по отношению к компонентам. Почти любая реакция является реакцией псевдонулевого порядка, если скорость реакции измеряется в начальный период. [7]
Необходимым условием для протекания данной реакции является щелочная среда. Обычно сочетание идет в пара-положение к ОН-группе. Если пара-положение занято заместителями, яеспособныии легко отщепляться ( например, алкил), диазосоставлнющая атакует ортоположение. [8]
Основными факторами, определяющими степень протекания данной реакции при каталитическом крекинге с неподвижным слоем катализатора, являются следующие. [9]
Если одного стехиометрического уравнения достаточно, чтобы описать протекание данной реакции, то ее относят к простым реакциям. [10]
Следовательно, рН среды не влияет на направление протекания данной реакции. [11]
Итак, тенденция к уменьшению внутренней энергии способствует протеканию данной реакции до конца в обратном направлении, а тенденция к увеличению вероятности состояния вызывает ее частичное протекание в прямом направлении. Вследствие одновременного действия обоих факторов часть азото-кислородной смеси при нагревании превращается в NO и устанав ливается равновесие между исходными веществами и продуктом реакции. [12]
Итак, тенденция к уменьшению внутренней энергии способствует протеканию данной реакции до конца в обратном направлении, а тенденция к увеличению вероятности состояния вызывает ее частичное протекание в прямом направлении. Вследствие одновременного действия обоих факторов часть азото-кислородной смеси при нагревании превращается в NO и устанавливается равновесие между исходными веществами и продуктом реакции. [13]
Итак, тенденция к уменьшению внутренней Энергии способствует протеканию данной реакции до конца в Обратном направлении, а тенденция к увеличению вероятности со - стояния вызывает ее частичное протекание в прямом направлении. [14]
Итак, тенденция к уменьшению внутренней энергии способствует протеканию данной реакции до конца в обратном направлении, а тенденция к увеличению вероятности со стояния вызывает ее частичное протекание в прямом направлении. Вследствие одновременного действия обоих факторов часть азото-кислородной смеси при нагревании превращается в NO и устанавливается равновесие между исходными веществами и продуктом реакции. [15]
Страницы: 1 2 3 4