Самопроизвольное протекание - реакция
Cтраница 3
Потенциал Н может быть достаточен для самопроизвольного протекания реакции ( 2) в правую сторону. [31]
Термодинамические расчеты указывают только на возможность самопроизвольного протекания реакции при данных условиях. Но под действием сопротивления внешней среды, например из-за кинетического сопротивления, реакция может находиться в квазиравновесном состоянии. Так, синтез воды из водорода и кислорода не идет при обычных условиях, хотя и является возможным на основании термодинамических расчетов. Такой синтез возможен с участием катализаторов. [32]
В каких случаях при определении направления самопроизвольного протекания реакции необходимо учитывать не только стандартные электродные потенциалы электрохимических систем, но и концентрации реагентов. [33]
Отрицательный знак ДС ( указывает на возможность самопроизвольного протекания реакции ( 1); положительный знак Д02 означает, что реакция ( 2) в указанных условиях протекать не может. [34]
Отрицательный знак ДО) указывает на возможность самопроизвольного протекания реакции ( 1); положительный знак Д02 означает, что реакция ( 2) в указанных условиях протекать не может. [35]
Итак, чтобы ответить на вопрос о возможности самопроизвольного протекания реакции слева направо или, наоборот, справа налево, необходимо знать состав реакционной смеси в момент ее приготовления и константу равновесия при данной температуре. [36]
Таким образом, при низких температурах критерием направления самопроизвольного протекания реакции ориентировочно ( в первом приближении) может служить знак теплового эффекта реакции, а в случае высоких температур - знак изменения энтропии. [37]
Отрицательный знак AG i, указывает на возможность самопроизвольного протекания реакции ( 1); положительный знак AG 2 означает, что реакция ( 2) в указанных условиях протекать не может. [38]
Итак, чтобы ответить на вопрос о возможности самопроизвольного протекания реакции слева направо или, наоборот, справа налево, необходимо знать состав реакционной смеси в момент ее приготовления и константу равновесия при данной температуре. [39]
В этой главе теоретически объясняются некоторые представления о самопроизвольном протекании реакций и о равновесии, которые были изложены в виде наблюдаемых фактов в гл. Сначала мы познакомились с константами равновесия как с чисто экспериментальными численными величинами, которые удобно использовать для предсказания поведения химической реакции после ее протекания в течение достаточно долгого времени. Нам еще не были известны способы вычисления константы равновесия по данным о других измеряемых свойствах химических веществ. [40]
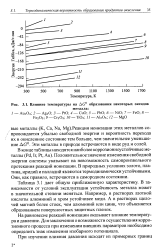 |
Влияние температуры на ДС образования некоторых оксидов. [41] |
Положительное значение изменения свободной энергии системы указывает на невозможность самопроизвольного протекания реакций ионизации. В природных условиях золото, платина, иридий и палладий являются термодинамически устойчивыми. Они, как правило, встречаются в самородном состоянии. [42]
Определим необходимую степень вакуумирования, которая обеспечила бы возможность самопроизвольного протекания реакции восстановления ниобия при Г1200 К. [43]
Пользуясь данными табл. 5 приложения, установить, возможно ли самопроизвольное протекание реакции 4А1 ЗС02 2А12О3 ЗС. [44]
Пользуясь данными табл. 5 приложения, установить, возможно ли самопроизвольное протекание реакции 4А1 ЗСО2 2А12О3 ЗС. [45]
Страницы: 1 2 3 4