Параллельное протекание - реакция
Cтраница 1
 |
Зависимость & Набл от концентрации вступающего лиганда. L-Вг - ( / и ОН - ( 2. [1] |
Параллельное протекание реакции по двум направлениям: через стадию акватации ( сольватации) и путем непосредственного замещения - встречается довольно часто. [2]
В предположении о параллельном протекании реакций 1 - 4 рассчитаны количества фтора, вступившего в реакцию. В работе [296] показано, что расчетные и экспериментальные количества фтора удовлетворительно совпадают. [3]
В других случаях наблюдается параллельное протекание реакции по двум маршрутам, причем распределение тока по ним зависит от условий опыта - от состава раствора, обработки поверхности электрода и др. Наличие посторонних примесей в растворе способствует, как правило, образованию пероксида. [4]
Полученное уравнение 5.8 учитывает параллельное протекание реакций деструкции ( деградации) и деполимеризации ПИБ на ионных и радикальных активных центрах одновременно, но не позволяет судить о причинах различия в селективности процесса по выходу мономера в присутствии катализаторов. [5]
 |
Микроструктура полиметилметакрилата, образующегося под действием производных хрома65. [6] |
Характер изменения микроструктуры полимера с конверсией ( позволяет допустить параллельное протекание реакций роста цепи на двух различных типах активных центров с изменением относительной роли каждого направления в ходе процесса. Сопоставление результатов, относящихся к инициатору IV и к перекиси бензонла, делает правдоподобным вывод о том, что одним из этих направлений является радикальная полимеризация, удельный вес которой в общей сумме превращений постепенно уменьшается. [7]
Электроосаждение большинства металлов и сплавов из водных растворов сопровождается параллельным протеканием реакции выделения водорода. В зависимости от рН раствора на электроде происходит разряд либо ионов гидроксо-ния, либо молекул воды. [8]
В заключение этого параграфа укажем, что двойственный характер химических процессов в электрическом разряде, проявляющийся в параллельном протекании реакций разложения и реакций синтеза, в той или иной мере свойственен всем углеводородам ( а также и соединениям других классов), насколько об этом можно судить по составу продуктов реакции, а также по составу ионов, устанавливаемому при помощи масс-спектрометра. [9]
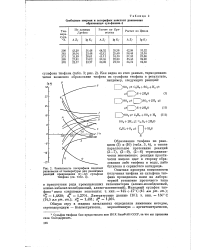 |
Зависимость логарифмов констант. [10] |
Образование тиофена по реакциям ( 3) и ( 10) ( табл. 3, 4), а также параллельное протекание реакций ( 2 - 7), ( 2 - 9), ( 2 - 6) термодинамически невозможно: реакция практически нацело идет в сторону образования либо тиофена и воды, либо бутилена и сернистого ангидрида. [11]
I было показано, что протонирование приводит к активации сернистой молекулы, облегчающей ее превращение. Параллельное протекание реакций превращения углеводородов и сернистых соединений в присутствии крекирующего катализатора, о котором сообщалось в работах [356, 426], вероятно, происходит потому, что эти две реакции ускоряются протонами, имеющими различную силу; не исключено, однако, участие в реакции крекинга сернистых соединений и апротонных центров ( см. гл. Вследствие протонирования атомов углерода алкилтиофенов становится возможным протекание реакций миграции алкильных групп в тиофеновом кольце и их отрыв от кольца. Эти реакции аналогичны реакциям превращения алкилбензолов. Таким образом, те причины, которые вызывают дезактивацию кислотного катализатора сернистым соединением, могут способствовать его собственному превращению. [12]
Величины oi, 02, Pi и fa, вычисленные для температур от 470 до 500 С, показали, что коэффициенты торможения оказались немного больше единицы. Кажущиеся энергии активации параллельных реакций ароматизации и газообразования ( гидрокрекинга), вычисленные по постоянным скорости для интервала температур от 470 до 500 С, были соответственно равны 22000 и 45000 кал / моль, что корреспондировалось с наблюдениями работы [58], Применение кинетических уравнений типа Фроста принципиально возможно и при рассмотрении параллельного протекания реакций ароматизации - дегидрирования нафтеновых углеводородов и дегидроциклизации парафиновых углеводородов. Степени превращения этих компонентов сырья должны вычисляться, исходя из остатка их в катализатах рифор-минга. [13]
Семеновым [7] развивалось представление о том, что гетерогенно-каталитические реакции, возможно, включают в себя цепные стадии. Ре-ал-вно существующие автокаталитические реакции, по-видимому, в большинстве случаев также представляют сочетания с другими типами. Это следует из того, что для начала автокаталитической реакции требуется присутствие катализатора в начале реакции или же параллельное протекание реакции по некаталитическому механизму. [14]
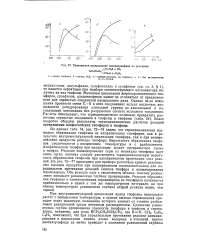 |
Равновесное превращение диэтилсульфида по реакциям. [15] |
Страницы: 1 2