Протонирование - молекула
Cтраница 1
Протонирование молекулы обычными кислотами практически не происходит, расщепить 5 - kv 3s - s - L. JJjl связь С-О не удается. Только при температуре выше 220 С при взаимодействии с А1С13 диариловые эфиры постепенно расщепляются. [1]
Реакция начинается с протонирования молекулы карбонильного соединения. В качестве основного центра выступает атом кислорода ок-согруппы, имеющий неподеленную пару электронов. В образовавшемся катионе заряд делокализован на атомах кислорода и углерода карбонильной группы. Резонансные ( мезомерные) структуры в данном случае демонстрируют распределение электронной плотности в катионе. [2]
 |
Прибор для получения аммиака. [3] |
Процесс можно рассматривать как протонирование молекулы аммиака, так как последняя является лучшим акцептором протона, чем молекула воды. [4]
Восстановительному процессу может способствовать протонирование молекулы азота или образование водородной связи с растворителем. [5]
При растворении ароматических углеводородов в жидком фтороводороде происходит протонирование молекулы ароматического углеводорода с образованием аренониевого иона, и получаются комплексы другого типа - а-комплексы. [6]
Сверхкислоты используют для разных целей, чаще всего дляа протонирования молекул, которые в обычных условиях не являются основаниями, например, ароматических углеводородов. [7]
Существенно, что свободно-радикальная деструкция гидропероксидов активируется кислотами [208] в результате протонирования молекул инициаторов с последующим гомолизом кислород-кислородной связи. [8]
Из схемы ( 3) видно, что первая стадия реакции - протонирование молекулы алкана, процесс, типичный для кислотного катализа - завершается во второй стадии восстановлением присоединившегося протона за счет окисления органической молекулы до карбониевого иона. Таким образом, в области очень высокой кислотности среды граница между кислотно-основными и окислительно-восстановительными процессами стирается. [9]
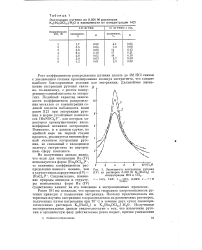 |
Зависимость экстракции рутения. [10] |
Рост коэффициентов распределения рутения вплоть до 4М НС1 связан с увеличением степени протонирования молекул экстрагента, что создает наиболее благоприятные условия для экстракции. [11]
Самым надежным критерием отнесения полосы к переходу с участием несвязывающих электронов является ее исчезновение при протонировании молекулы в кислых средах. [12]
Формально реакция напоминает процесс SNl, и в этом случае, казалось бы, вновь актуальным становится вопрос о месте протонирования молекулы сложного эфира. Показано, однако, что сложные эфиры и третичных спиртов в ходе кислотно-катализируемого гидролиза также протонируются по атому кислорода карбонильной группы. [13]
В случае протолиза свинецорганических соединений показано, что константа скорости псевдсмономолекулярной реакции при относительно низких концентрациях кислоты меняется линейно с концентрацией кислоты. Это означает, что лимитирующей стадией в этих условиях является протонирование молекулы элементоорганиче-ского соединения. [14]
Тропой, 1 3 5-щшлогептатриенон - довольно сильное основание, дающее соли с такими кислотами, как соляная. Столь необычная основность электронной пары карбонильной группы объясняется стабильностью ароматического катиона, образующегося при протонировании молекулы. В этом катионе бл-электронов делокализованы на семи р-орбиталях. [15]
Страницы: 1 2