Протонирование - молекула
Cтраница 2
Изменение наклона поляризационной кривой при ее параллельном сдвиге с изменением рН, вероятно, связано с уменьшением заполнения поверхности блокирующими частицами. Однако эта схема пока является не более чем рабочей гипотезой, поскольку отсутствуют непосредственные данные о протонировании молекулы О2 на электродной поверхности. [16]
Существует ряд методов, посредством которых боковая углеродная цепь, длинная или короткая, может быть непосредственно введена в незамещенное бензольное кольцо, и все эти методы, несмотря на кажущееся внешнее различие, имеют ряд существенных общих черт. В любом из методов атом углерода, который выступает в роли электрофила по отношению к ароматическому кольцу, либо имеет электронодефицитный характер за счет наличия соседнего сильно электроотрицательного атома, либо способен стать элек-тронодефицитным за счет протонирования молекулы реагента. Кроме того, даже если связь этого атома углерода с электроотрицательным атомом очень сильно поляризована, атом углерода все равно еще не является достаточно сильным электрофилом для того, чтобы разорвать я-систему бензола. Этот факт лишний раз подтверждает утверждение, уже высказанное в гл. [17]
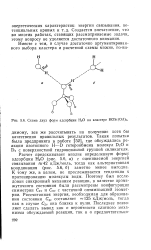 |
Схема двух форм адсорбции НгО на кластере HOSi ( OA3. [18] |
Такая попытка была предпринята в работе [52], где обсуждались реакции изотопного Н - D гетерообмена молекул D2O и D2 с поверхностной гидроксильной группой силикагеля. Расчет предсказывает вполне определенную форму адсорбции Н2О ( рис. 5.6, а) с оцениваемой энергией связывания 42 кДж / моль, тогда как альтернативная координация ( рис. 5.6, б) заметно менее выгодна. К тому же, в целом, не прослеживается тенденции к протонированию молекулы воды. Поэтому был исследован синхронный механизм реакции, в качестве промежуточного состояния были рассмотрены конфигурации симметрии C2v и С3с с частичной оптимизацией геометрии. Рассчитанная энергия, необходимая для образования состояния С3 составляет - 125 кДж / моль, тогда как в случае C % v она близка к нулю. [19]
Они постоянны, только если постоянна эта концентрация. В аналитической химии часто пользуются зависимостью реальной константы Кг от концентрации [ S3I для выяснения влияния побочного равновесия на главное равновесие. Например, если главным выступает равновесие образования аммиакатов, а побочным - равновесие протонирования молекул аммиака, зависимость / С от концентрации ионов водорода ( вещество S3) или от рН показывает влияние кислотности среды на устойчивость аммиакатов. [20]
Аминокислоты, являющиеся внутренними солями, практически не испаряются в масс-спектрометре. Для повышения летучести обычно их переводят в метиловые или этиловые эфиры. В ряде случаев осуществляют также защиту аминогруппы путем ее ацетилирования или трифторацетили-рования. При этом кроме молекулярного иона наблюдаются зачастую даже более интенсивные пики ионов ( М 1), образующиеся вследствие легкого протонирования молекулы, например влагой в приборе, или вследствие йономолекулярных реакций между молекулами самого вещества. [21]
Страницы: 1 2