Протопорфирин
Cтраница 2
Близок по строению к протопорфирину ( одна винильпая группа заменена на формильную) хло-рокруоропорфирин - простетич. В хлоропластах зеленых частей растений наряду с каротином и ксантофиллом содержатся в соотношении 3: 1 два пигмента, близкие но строению к пигментам крови: сине-зеленый хлорофилл а ( XVIII, R - СН3) и желто-зеленый хлорофилл б ( XVIII, НСНО), играющие важнейшую роль и фотосинтезе. Кроме того, в растениях содержится про-тохлорофилл а ( XVIII, RC2H5), у к-рого кольцо А дегидрировано. [16]
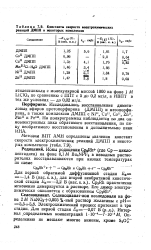 |
Константы скорости влектрохимических реакций ДМПП и некоторых комплексов. [17] |
Исследовалось восстановление диметн-ловых эфиров протопорфирина ( ДМПП) и мезопорфи-рина, а также комплексов ДМПП с Ni11, Си11, Со11, Zn. [18]
Близок по строению к протопорфирину ( одна винильная группа заменена на формильную) хло-рокруоропорфирин - простетич. В хлоропластах зеленых частей растений наряду с каротином и ксантофиллом содержатся в соотношении 3: 1 два пигмента, близкие по строению к пигментам крови: сине-зеленый хлорофилл а ( XVIII, 11СН3) и желто-зеленый хлорофилл б ( XVIII, RCHO), играющие важнейшую роль в фотосинтезе. Кроме того, в растениях содержится про-тохлорофилл а ( XVIII, RC2H5), у к-рого кольцо А дегидрировано. [19]
После этого в молекулу протопорфирина включается магний или железо с образованием Mg - или Fe-протопорфирина. Железосодержащий протопорфирин служит непосредственно в качестве простетической группы некоторых гемопротеидов ( фиг. [20]
При отщеплении иона железа образуется протопорфирин, который при декарбоксилировании и гидрировании превращается в этиопорфи-рин. [21]
Железо может быть введено в протопорфирин IX без участия ферментов путем нагревания с солью железа ( II) в уксусной кислоте или в пиридине. При физиологических значениях рН, однако, неферментативное включение железа осуществляется довольно медленно. Железо вообще не включается в порфириногены, конформа-ция пиррольных колец которых не столь идеально соответствует образованию комплекса, как планарная сопряженная кольцевая система порфирина. В то же время цинк способен связываться с порфириногенами и порфиринами как ферментативным путем, так и без участия ферментов; нежелательное образование комплексных соединений с цинком затрудняет изучение железопорфиринов. [22]
Магний может внедряться уже в протопорфирин IX, образуя маг-нийпротопорфирин. [23]
Гидрирование двух активных двойных связей протопорфирина приводит к мезопорфирину. [24]
Аналогичный способ очистки диметилового эфира протопорфирина предложен в работе [117]: 20 г неочищенного образца наносили на колонку, содержащую 450 г оксида алюминия, и быстро элюировали хлороформом. В этих условиях структурные повреждения винильных групп протопорфирина минимальны. Очень широкие возможности хроматографии на оксиде алюминия продемонстрированы в работе [63], в которой описана очистка диметиловых эфиров некоторых производных дейтеропорфирина (11.11), содержащих разнообразные заместители R, и R2: - СН2СООН, - СН2СН2СООН, - Br, - NO2 и - СМ. В каждом случае хроматография на оксиде алюминия ( около 35 г сорбента на 1 г порфирина) в хлороформе, который, вероятно, содержал в качестве стабилизатора этанол, позволяла получить достаточно чистый препарат. Позднее [118] на том же сорбенте удалось разделить эти изомеры. Для препаративного выделения порфиринов, связанного с - очисткой основного компонента от небольших количеств приме-сей, оксид алюминия можно брать из расчета 50 г на 1 г образца, а часто бывает достаточно и половины указанного количества сорбента. Однако в более сложных случаях следует использовать значительно большее количество оксида алюминия - вплоть до 500 г на 1 г образца. [25]
Одним из наиболее важных порфиринов является протопорфирин. Основные контуры его полностью повторяют структуру этиопорфирииа с той разницей, что вместо двух этиловых групп протопорфирин содержит, два пропионовых остатка. Комплексное соединение протопор-фирина с двухвалентным железом называется г ем ом, а с трехвалентным - гематином. [26]
На каждый включившийся атом азота глицина в протопорфирин включаются два а-углеродных атома глицина. [27]
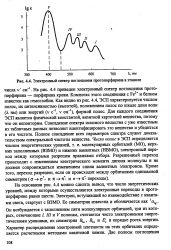 |
Электронный спектр поглощения протопорфирина в этаноле. [28] |
На рис. 4.4 приведен электронный спектр поглощения протопорфирина - порфирина крови. Комплекс этого соединения с Fe2 и белком известен как гемоглобин. Как видно из рис. 4.4, ЭСП характеризуется числом полос, их интенсивностью ( высотой), положением полос по шкале длин волн ( X нм) или энергий ( v с 1, v см 1), формой полос. Для каждого соединения ЭСП является физической константой, визитной карточкой вещества, потому что он неповторим. Совпадение спектра искомого вещества с уже известным из табличных данных позволяет идентифицировать это вещество и убедиться в его чистоте. Полное совпадение всех параметров спектра служит доказательством спектральной чистоты вещества. МО), верхних заполненных ( ВЗМО) и нижних вакантных ( НВМО), электронный переход между которыми разрешен правилами отбора. Разрешенный переход происходит с изменением электрического момента диполя молекулы и не должен сопровождаться изменением спина валентных электронов. [29]
Недостаточность железа также приводит к повышению концентрации протопорфирина в эритроцитах. Эритроци-тарные ферменты ALA-D и П5Н весьма чувствительны к ин-гибирующему действию свинца. При уровне свинца в крови 10 - 40 мкг / 100 мл наблюдается существенная отрицательная корреляция между активностью обоих ферментов и концентрацией свинца в крови. [30]
Страницы: 1 2 3 4