Энергетический профиль
Cтраница 2
Необходимо подчеркнуть, что энергетические профили типа показанных На рис. 2.2 и 2.3, не есть нечто абсолютное, жестко задаваемое только структурой рассматриваемых соединений. Влияние этих факторов на возможность реализации того или иного пути реакции в общем поддается рациональной интерпретации. [16]
Пособие предназначено для техникумов энергетического профиля. Цель пособия состоит в развитии навыка чтения и понимания английской литературы по радиоэлектронике и радиотехнике. Пособие может быть использовано также для развития элементарных навыков говорения на темы, связанные с этими специальностями. [17]
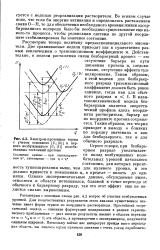 |
Электрон-протонные термы с учетом основного [ Ui ( 0J и первого возбужденного [ Ui ( 1 ] колебательных состояний протона. [18] |
В кван-товомеханической модели безбарьерным является энергетический профиль вдоль координаты растворителя, барьер же по координате протона сохраняется. [19]
На рис. 155 схематически показан энергетический профиль процесса. [20]
Электроматериаловедение в профессионально-технических учебных заведениях энергетического профиля является общетехнической дисциплиной и служит ( вместе с другими курсами) основой для изучения специальных предметов. [21]
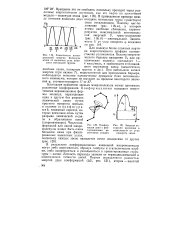 |
Зависимость потенциальной энергии Молекулы этана от величины угла поворота метильной группы.| Энергия активации вращения в зависимости от угла поворота звена. [22] |
Для молекул более сложных картина энергетического профиля соответственно усложняется. [23]
На рис. 22 - 3 дан энергетический профиль идеализированного нуклео-филыюго замещения в ароматическом ряду. Как и в случае большинства реакций электрофнлыюго замещения в ароматическом ряду, скорость процесса определяется скоростью нарушения ароматической я-системы. [24]
Как отмечалось в предыдущем разделе, энергетический профиль этой элементарной стадии можно построить, если известны частоты нескольких переходов в ИК-спектрах свободных гидроксильных групп или их комплексов с реагирующими молекулами. Соответствующие данные имеются и для гомогенных, и для гетерогенных систем. В первую очередь рассмотрим гомогенные системы, поскольку они изучены более детально. [25]
На рис. 1.8 показаны энергетические диаграммы ( энергетические профили) эндотермической и экзотермической реакций. [26]
Книга рассчитана на специалистов научно-исследовательских и проектно-конструкторских учреждений энергетического профиля. [27]
Весьма полезным для понимания 8м1 - замещения является рассмотрение энергетического профиля ( рис. 5 - 4) приведенного выше идеализированного процесса превращения алкилиодида в алкилбромид. Из двух последовательных стадий ( ионизации и рекомбинации ионов) ионизация является наиболее трудной. Характерной особенностью активированного комплекса, распад которого ведет к образованию ионов, является увеличение длины связи между углеродом и иодом. Рассматриваемый комплекс образуется только из одной частицы ( R-I), и поэтому, как отмечалось выше, реакцию в целом называют мономолекулярной. [28]
Ола впервые рассмотрел переходные состояния так, что в общепринятом энергетическом профиле он перевернул максимумы, соответствующие я - и 0-комплек-сам. Однако он подчеркнул, что разделение на отдельные энергетические максимумы, приводящее к разделению л - и сг-комплексов, не обязательно. Он обсудил такую возможность, что, например, при нитровании и бензили-ровании отдельные минимумы, соответствующие некоторым промежуточным соединениям, могут не появиться, и на профиле энергии будут находиться только два максимума. Первый максимум будет соответствовать переходному состоянию, которое так рано появляется на координате реакции, что становится похожим на ориентированный я-комплекс. Второй максимум соответствует отщеплению протона. Реакции с очень сильными электрофильными агентами имеют ранние переходные состояния, которые могут быть сходными с я-комплексами; это согласуется с точкой зрения Дьюара. Если эти реакции протекают, как изображено на рис. 1, то стадия, определяющая скорость реакции, настолько удалена от стадии разрыва связи С - Н, что исключается возможность появления первичного изотопного эффекта. Согласно Ола, небольшие эффекты, которые наблюдались во всех этих реакциях, должны быть определенно отнесены ко вторичным изотопным эффектам. [29]
Лица, обучающиеся в высших или средних специальных учебных заведениях энергетического профиля, решением администрации могут освобождаться от курсового обучения на предприятии, за исключением курсовых занятий по изучению вновь вводимого оборудования и вопросов техники безопасности. [30]
Страницы: 1 2 3 4 5