Энергетический профиль
Cтраница 4
В типичном случае общего кислотного или общего основного катализа перенос протона от АН к R или от RH к В является самой медленной стадией общего многостадийного процесса ( разд. Энергетический профиль можно представить как результат наложения друг на друга отдельных параболических кривых потенциальной энергии для RH и В0Н, соответствующих растяжению связи R - Н при переходе от ( RH BO) к переходному состоянию ( R... [46]
Пересечение энергетических профилей приводит к нарушению пропорциональности между энергиями на разных участках пути реакции. [47]
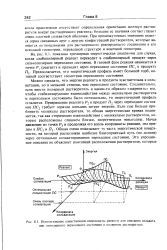 |
Использование единственной координаты реакции для описания сольвата ции пиполярного переходного состояния в полярном растворителе. [48] |
На рис. 8.1. показана трехмерная энергетическая диаграмма для случая, когда слабополярный реагент переходит в слабополярный продукт через сильнополярное переходное состояние. Предполагается, что энергетический профиль имеет большой горб, который соответствует геометрии переходного состояния. [49]
В кван-тово-механической модели безбарьерным является энергетический профиль вдоль координаты растворителя, барьер же по координате протона сохраняется. Таким образом, эта теория приводит к выводу о близких по порядку значениях х1 как для безбарьерного, так и для обычного разряда. [50]
 |
Различные профили потенциальной энергии для реакции электрофвль-лого замещении в ароматической ряду. [51] |
На рис 9.3 - обобщены идеи, представленные в разд. Признано существование по крайней мере четырех танов энергетических профилей для конкретных реакций электрофильного ароматического замещения. Для случая ( а) стадией, определяющей скорость реакции, является стадия генерации электрофила. [52]
При исследовании химотрипсина Бендер и Кеж-ди [16] показали, что константы скорости индивидуальных стадий ферментативного гидролиза эфиров триптофана находятся в соответствии с константой равновесия суммарного процесса. Для этого процесса, следовательно, может быть построен полный энергетический профиль. [53]
Вопрос о селективности химических реакций, имеющий первостепенное значение для практической химии, с теоретической точки зрения состоит в сравнении эффективности различных возможных каналов химической реакции, приводящих к разным продуктам, например к разным стереоизомерам, хотя различие может быть, конечно, и более фундаментальным. В свою очередь это приводит к квантовохимической задаче расчета энергетических профилей вдоль реакционных путей для рассматриваемых каналов реакции. Однако практическая реализация этой очевидной рекомендации сталкивается с громадными вычислительными трудностями, особенно для многоатомных систем, где многомерная ППЭ всей перестраивающейся молекулярной системы будет иметь очень сложную форму. [54]
 |
Энергетические профили некаталитической и каталитической реакций. EI - энергия активации некаталитической и. 2 - каталитической реакций. [55] |
VIII, принципиально возможно построить поверхность потенциальной энергии и представить себе энергетические профили путей некаталитической и каталитической реакций. Примерная теоретическая картина изображена на рис. ХИЛ. [56]
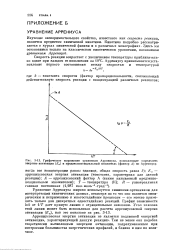 |
Графическое выражение уравнения Аррениуса, позволяющее определить энергию активации ( Еа и предэкспоненциальный множитель ( фактор А по Арренпусу. [57] |
Аррениусовская энергия активации не является подлинной энергией активации, характеризующей данную реакцию. Тем не менее она подобна теоретически вычисленным энергиям активации, подразумеваемым при построении большинства энергетических профилей, и близка к ним по величине. [58]
Эйринга, не зависят от температуры, и именно их следует использовать при сравнении энергетических профилей аналогичных реакций. [59]
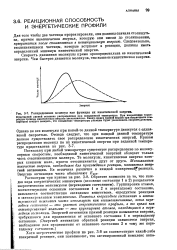 |
Распределение молекул как функция их кинетической энергии. [60] |
Страницы: 1 2 3 4 5