Процесс - енолизация
Cтраница 2
Его роль заключается в ускорении процесса енолизации карбонильного соединения. [16]
При повышении температуры количество енольной формы уменьшается. Определение зависимости состава равновесия от температуры показало, что в газообразном состоянии процесс енолизации экзотермичен, и энтропия при енолизации уменьшается. При енолизации ацетилацетона разность АЯ - Г AS при повышении температуры примерно постоянна, при енолизации ацетоуксусного эфира при 25 С АЯ TAS и обе формы находятся в равном количестве. При повышении температуры большее значение имеет энтропийный член и содержание кетонной формы больше, чем енольной; при температурах ниже 25 С - наоборот. [17]
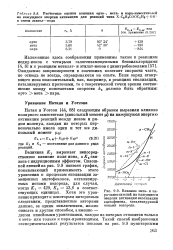
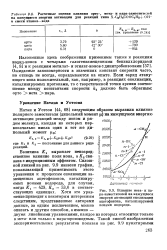
Величина Кх выражает непосредственное влияние поля иона, а К2 связана с индукционным эффектом. Сплошной линией на рис. 9.9 нанесен график, показывающий применимость этого уравнения к процессам енолизации замещенных ацетофенонов, катализируемых ионами водорода, для случая, чкогда Кг 429, К2 53 6 в соответствующих единицах. Хотя это уравнение приводит к некоторым интересным следствиям, представленные авторами данные, за одним исключением, можно описать и другим способом, а именно - двумя линейными уравнениями, каждое из которых относится только к мета - или только к пара-производным. [19]
Величина К выражает непосредственное влияние поля иона, а К % связана с индукционным эффектом. Сплошной линией на рис. 9.9 нанесен график, показывающий применимость этого уравнения к процессам енолизации замещенных ацетофенонов, катализируемых ионами водорода, для случая, когда Кг 429, К2 53 6 в соответствующих единицах. [21]
Опыты показали [146], что как при большом избытке, так и при недостатке спирта в среде енолизации снижается выход аскорбиновой кислоты. Отмечено также, что при избытке спирта наряду со снижением выхода аскорбиновой кислоты повышается ее качество, а при недостатке спирта или при попадании воды в хлороформ аскорбиновая кислота получается в виде гранул и плохо промывается. Добавление больших количеств ацетона ( 20 %) ухудшает процесс енолизации и снижает выход. [22]
К ним относятся енолы, многие фенолы и соединения, способные к енолизации. Метилкетоны более активны в этой реакции, чем другие кетоны, однако, как это характерно и для других карбонильных соединений, при их бро-мировании наблюдается индукционный период. Это связано с тем, что выделяющийся бромистый водород действует как катализатор процесса енолизации. [23]
Последний загружают при непрерывном перемешивании. Затем в реакционную массу добавляют спиртовой раствор хлористого водорода из расчета 50 г хлористого водорода на 1 кг гидрата. Необходимо следить за тем, чтобы содержание спирта в реакционной массе составляло 0 22 л па I кг гидрата. После этого процесс енолизации и лактонизации считается законченным, реакционную массу охлаждают до 15 С и выгружают. [24]
Енольные формы р-дикетонов и р-кетоэфиров являются сопряженными системами, поэтому содержание енола относительно велико. Пентандион-2 4 ( ацетилацетон) содержит около 76 % еноль-ной формы в газовой фазе и около 80 % в чистой жидкости при 25 С. Ациклические р-дикетоны могут иметь цис - или транс-кон-фигурацию [ схема ( 12) ] относительно енольной двойной связи, причем ис-изомеры ( 25) и ( 26) являются хелатами и поэтому они гораздо устойчивее ту. Несимметричные дикето-ны могут иметь два структурно изомерных енола. В работе [37] приведены термодинамические данные для таутомерии многих Р - дикетонов и р-кетоэфиров. Процесс енолизации протекает экзотермически в газовой фазе, в неразбавленной жидкости и в растворе. Электроноакцепторные группы R, R и R увеличивают устойчивость кетоенольной формы по сравнению с дикетонной, тогда как алкильные группы и объемистые группы R понижают ее. [25]
Енольные формы р-дикетонов и р-кетоэфиров являются сопряженными системами, поэтому содержание енола относительно велико. Пентандион-2 4 ( ацетилацетон) содержит около 76 % еноль-ной формы в газовой фазе и около 80 % в чистой жидкости при 25 С. Ациклические р-дикетоны могут иметь цис - или транс-кон-фигурацию [ схема ( 12) ] относительно енольной двойной связи, причем цыс-изомеры ( 25) и ( 26) являются хелатами и поэтому они гораздо устойчивее транс-изомеров. Несимметричные дикето-ны могут иметь два структурно изомерных енола. В работе [37] приведены термодинамические данные для таутомерии многих Р - дикетонов и р-кетоэфиров. Процесс енолизации протекает экзотермически в газовой фазе, в неразбавленной жидкости и в растворе. Электроноакцепторные группы R, R и R увеличивают устойчивость кетоенолыюй формы по сравнению с дикетонной, тогда как алкильные группы и объемистые группы R понижают ее. [26]
Страницы: 1 2