Процесс - кристаллизация - жидкость
Cтраница 1
Процесс кристаллизации жидкости начинается с возникновения зародышей твердой фазы. При этом не любой возникший зародыш способен к самостоятельному существованию и дальнейшему росту. [1]
Недавно математическое моделирование было применено к процессу кристаллизации жидкости. Моделирование показало, что кристаллы с острыми кончиками росли быстро и обладали большой устойчивостью в отличие от плоских образований, росших медленно и отличавшихся меньшей стабильностью. Однако, когда эти медленно растущие формы подвергались воздействию со стороны, они имели тенденцию распадаться на острые, быстро растущие осколки. [2]
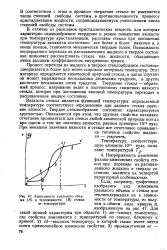 |
Зависимость удельного объема ( А и теплоемкости ( В стекол от температуры. [3] |
В соответствии с этим в процессе твердения стекол не изменяется число степеней свободы системы, в противоположность процессу кристаллизации жидкости, сопровождающемуся уменьшением числа степеней свободы системы. [4]
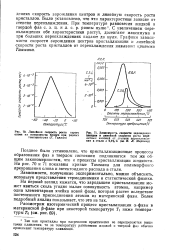 |
Линейная скорость роста Серого.| Зависимость скорости зарождения центров и лияейной скорости роста пере-литных колоний от степени переохлажде-аия в стали с 0 8 % С ( по Я. Л. Маркину. [5] |
Позднее было установлено, что кристаллизационные процессы образования фаз в твердом состоянии подчиняются тем же общим закономерностям, что и процессы кристаллизации жидкости. На рис. 70 и 71 показаны кривые Таммана для полиморфного превращения олова и эвтектоидного распада в стали. [6]
В основе проявления прочности лежит энергия, порождаемая при конденсации свободных молекул в жидкости, и энергия, порождаемая в процессе кристаллизации жидкости. Прочность материала и характер его деформации зависят как от особенностей соединения в нем атомных остатков, так и от способа воздействия на материал внешней нагрузки, приводящей к различным закономерностям развития и распределения в материале напряжений: к отталкивающим воздействиям атомных остатков при сжатии, проявлению сил их притяжения при растяжении, охрупчиванию при скоростном нагружении или сложным сочетаниям в объеме тех или иных взаимодействий, имеющихся, например, при усталостной деформации, когда различную характеристику могли бы иметь амплитуда и частота. [7]
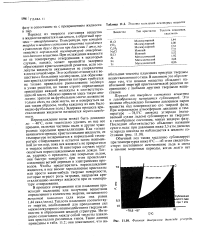 |
Теплота плавления некоторых веществ.| Фазовая диаграмма диоксида углерода. [8] |
Переохлаждение воды может быть доведено до - 40 С, если тщательно удалить из нее все примеси, включая частицы пыли и другие чужеродные зародыши кристаллизации. Как только начинается процесс кристаллизации жидкости, ее температура возвращается к нормальной температуре отвердевания и остается затем неизменной до тех пор, пока вся жидкость не превратится в твердое вещество. В некоторых случаях могут оказаться переохлажденными капли дождя. Тогда, ударяясь о предметы, уже покрытые льдом, они быстро замерзают; при этом происходит оледенение ветвей деревьев и электрических проводов. Чтобы предотвратить переохлаждение жидкости, в нее вносят зародышевые кристаллы или просто какие-нибудь твердые поверхности, которые играют роль затравки, направляя кристаллизацию молекул жидкости при ее температуре отвердевания. [9]
Диффузионное превращение происходит по механизму образование зародыша и рост новой фазы. Этот тип превращения подчиняется тем же общим закономерностям, что и процессы кристаллизации жидкости ( см. гл. Существуют некоторые особенности, связанные с твердым состоянием исходной и образующейся фаз и относительно низкой температурой превращений. Возникновение зародышей обеспечивается в результате флуктуационного повышения энергии в отдельных группах атомов. При превращении в сплавах образуются фазы, отличающиеся по составу от исходной, поэтому для образования зародыша необходимо также наличие флуктуации концентрации. Последнее затрудняет образование зародышей новой фазы, особенно если ее состав сильно отличается от исходной. Другой фактор, затрудняющий образование зародыша новой фазы, связан с упругой деформацией фаз, которая обусловлена различием удельных объемов исходной и образующейся фаз. Энергия упругой деформации увеличивает свободную энергию и, подобно поверхностной энергии, вносит положительный вклад в баланс энергии. Критический размер зародышей и работа их образования уменьшаются с увеличением степени переохлаждения ( или перегрева) по отношению к равновесной температуре 7 р, а также при уменьшении поверхностной энергии зародыша. [10]
Процесс твердения стекол не связан с появлением в системе новой фазы. Этим твердение стеклообразных расплавов резко отличается от кристаллизации, при которой процесс перехода жидкость-твердое вещество всегда сопровождается появлением в системе новой фазы. В соответствии с этим в процессе твердения стекол не изменяется число степеней свободы системы, в противоположность процессу кристаллизации жидкости, сопровождающемуся уменьшением числа степеней свободы системы. [11]
Величина амплитуды тепловых колебаний частиц сильно зависит от природы химической связи между ними. Металлические, преимущественно ионные химические связи между атомами, слабые ван-дер-ваальсовы связи между молекулами создают ситуацию, при которой амплитуды тепловых колебаний существенны, и упорядочение при прохождении остывающего расплава через точку плавления неизбежно. В таких веществах, по мнению Мюллера [114-116], увеличение расстояния между частицами приводит ( рис. 13, а) к сравнительно слабому и постепенному уменьшению прочности ( энергии) связи. Это и является причиной перегруппировки частиц в процессе кристаллизации жидкости. В работах Мюллера положено начало глубокому изучению природы химической связи в стекле и стеклообразующих жидкостях. [12]
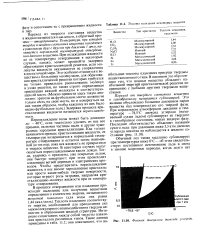 |
Теплота плавления некоторых веществ.| Фазовая диаграмма диоксида углерода. [13] |
Переход из твердого состояния вещества в жидкое называется плавлением, а обратный процесс - отвердеванием. Температура, при которой твердое и жидкое состояния вещества находятся в равновесии друг с другом при давлении 1 атм, называется нормальной температурой отвердевания данного вещества. При охлаждении жидкости до ее температуры отвердевания в некоторых случаях, однако, может произойти задержка образования кристаллической решетки, если молекулы жидкости оказываются не упорядочены в достаточной мере. Это особенно относится к веществам с большими молекулами, для образования кристаллической решетки которых требуется не только правильное расположение молекул в узлах решетки, но также строго определенная ориентация каждой молекулы в соответствующем ей месте. Можно привести здесь такую аналогию: зрители на футбольном матче должны не только сесть на свои места, но и повернуться на них таким образом, чтобы каждому из них было видно футбольное поле. Задержка процесса кристаллизации жидкости называется переохлаждением. [14]
Страницы: 1