Процесс - нейтрализация - кислота
Cтраница 1
Процесс нейтрализации кислот аммиаком является одной из основных стадий производства при получении минеральных удобрений, содержащих азот в аммиачной и нитратной формах. [1]
Процесс нейтрализации кислот регулируется автоматически регулятором соотношения потоков. Датчиком служит рН - метр на линии умягченной воды. [2]
Продолжительность процесса нейтрализации кислоты изменяется в зависимости от литологических особенностей породы, особенностей и концентрации кислотного раствора, температуры и давления, при которых происходит реакция. [3]
В процессе нейтрализации кислот и оснований одинаковой нормальности, но различной силы титруемый раствор становится нейтральным раньше или лозже достижения эквивалентной точки. [4]
 |
Характеристика аппарата САМ. [5] |
По гипотезе [181], механизм процесса нейтрализации кислот аммиаком в струйном реакторе является циклично-пульсирующим во времени и характеризуется отсутствием ламинарного диффузионного подслоя. [6]
По сравнению с коллоидальной гидроокисью алюминия процесс нейтрализации кислоты амберлитом Ш-4 идет значительно быстрее. [7]
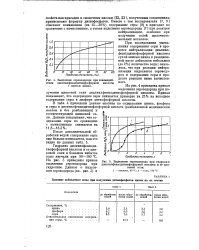 |
Выделение сероводорода при гидролизе диоктилфенилдитиофосфорной кислоты и ее цинковой соли. [8] |
При исследовании уменьшения содержания серы в процессе нейтрализации диалкил-фенилдитиофосфорной кислоты сухой окисью цинка к реакционной массе добавляли небольшое ( до 2 %) количество воды; оказалось, что при реакции нейтрализации выделяется сероводород и содержание серы в продукте реакции ниже вычисленного. [9]
При проведении электролиза при строгом постоянстве ia измеряют продолжительность процесса нейтрализации кислоты тэ. [10]
Повышенное содержание присадки в масле объясняется интенсивным ее расходованием в процессе нейтрализации кислот. [11]
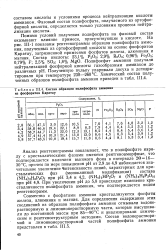 |
Состав образцов полифосфаш аммония из фосфоритов Каратау. [12] |
Фазовый состав полифосфата, получаемого из ортофос-форной кислоты, определяется только условиями процесса нейтрализации кислоты. [13]
Константа Kw имеет большое значение в аналитической химии, помогая разобраться в процессе Нейтрализации кислот и оснований. Вода, находясь на воздухе, поглощает двуокись углерода, что ведет к повышению концентрации водородных ионов за счет образования угольной кислоты. Концентрация водородных ионов может возрасти при этом в - 20 раз. Вода же, хранящаяся в стеклянной посуде, растворяет стекло, приобретая щелочную реакцию. [14]
Константа Kw имеет большое значение в аналитической химии, помогая разобраться в процессе нейтрализации кислот к оснований. Вода, находясь на воздухе, поглощает двуокись углерода, что ведет к повышению концентрации водородных ионов за счет образования угольной кислоты. Концентрация водородных ионов может возрасти при этом в - 20 раз. Вода же, хранящаяся в стеклянной посуде, растворяет стекло, приобретая щелочную реакцию. [15]
Страницы: 1 2