Процесс - окисление - кумол
Cтраница 1
Процесс окисления кумола в гидроперекись является первой стадией процесса производства фенола и ацетона из кумола, реализованного в промышленности в крупном масштабе. [1]
В процессе окисления кумола источники загрязнения воздушного бассейна - выбросы из колонны гидрогенизации, содержащие водород ( 15 г / т фенола) и оксид углерода ( 20 г / т фенола); выбросы из каталитического реактора, содержащие следы метил-стирола, оксид углерода ( 0 20 кг / т фенола) и фенол ( 1 5 кг / т фенола), а также поток из отпарной - колонны. [2]
Существуют также процессы окисления кумола воздухом в безводной среде, протекающие с меньшей конверсией в стадии окисления. В других методах основной целью является получение а-метилстирола, для чего гидроперекись кумола превращают в щелочной среде в диметилфенилкарбинол и дегидратируют последний. [3]
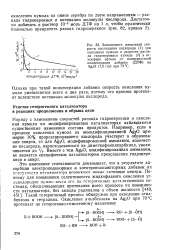
Изучено влияние температуры на процесс окисления кумола в присутствии смешанных катализаторов. При температурах 100, НО, 120, 130 С максимальная скорость накопления гидроперекиси достигается в начале процесса. При температурах 80, 90 С наблюдается индукционный период, максимальная скорость достигается спустя 4 - 6 часов окисления. Эти данные получены при окислении кумола в присутствии серебряно-бариевого и кадмий-бариевого катализаторов. При окислении кумола в присутствии медно-барие-вого катализатора максимальная скорость достигается при всех исследованных температурах в начале процесса. [4]
 |
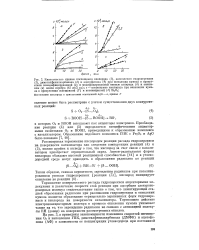
Зависимость выхода ацетофенона от глубины окисления.| Кинетические кривые накопления гидроперекиси в окисляющемся кумоле при введении ингибитора ( а-нафтиламина. [5] |
Гидроперекись кумила распадается в процессе окисления кумола при сравнительно высоких температурах. Энергия активации термического распада гидроперекиси зависит от ее концентрации, вида растворителя и наличия примесей. [6]
Наряду с изменением скоростей распада гидроперекиси и окисления кумола на модифицированных катализаторах наблюдаются существенные изменения состава продуктов. Например, если в процессе окисления кумола на немодифяцировавной Ag2O примерно 10 % прореагировавшего кислорода участвует в образовании спирта, то для Ag2O, модифицированной аммиаком, количество - кислорода, израсходованного на диметилфенилжарбинол, увеличивается до / з - Вместе с тем Ag2O, модифицированная аммиаком, не является специфичным катализатором превращения гидроперекиси в спирт. [8]
Именно по этой причине большинство промышленных реакторов работают при величинах съема ГПК от 30 кг / м3 в час до 50 кг / м в час, заведомо направляя реакцию по пути снижения селективности. Исключением является только ammoxidation - процесс сухого окисления кумола, в котором при величине ГПК 35 - 40 кг / м3 в час достигнута селективность около 95 % ( мол. [9]
Торможение поверхностного распада гидроперекиси акцепторными молекулами и увеличение скорости этой реакции при адсорбции электроно-донорных молекул свидетельствуют также о том, что лимитирующей стадией образования радикалов при разложении гидроперекиси и окислении кумола является образование отрицательно заряженных форм гидроперекиси и кислорода на поверхности катализатора. Тормозящее действие электроноакцепторньгх молекул в процессе окисления кумола указывает также на то, что зарождение радикалов не связано с активацией молекулы RH ( донор) на поверхности рассмотренных окислов. [11]
 |
Спектр ЭПР ради - следований, авторы рассчитали возможные кон-кала PhC ( CH3 200. образую - центрации этих радикалов в ходе реакции, щегося при окислении кумола. - r. [12] |
Лебедева и др. [20] из большого числа детально изученных в кинетическом отношении реакций жидкофазного окисления был специально выбран процесс окисления кумола, при котором ввиду больших стерических трудностей реакция рекомбинации перекисного радикала PhCH ( CH3) 2Ob, ведущего цепь, должна была оказаться очень замедленной, а стационарная концентрация соответственно очень высокой. [13]
В других работах [128, 130] установлено, что при окислении п - и лг-нсилолов кислородом воздуха в присутствии ряда катализаторов - стеарата свинца, кобальта и никеля - наибольшей активностью обладает соль кобальта. К такому же выводу пришел Рушо [154] при изучении катал и-тической активности хелатных комплексов бис ( 2 2 - гидрО бензи-лиден) этилендиамина и тяжелых металлов в процессе окисления кумола до гидропероксидов. [14]
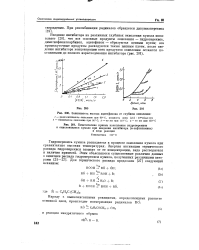
 |
Зависимость отношения концентрации растворенного кислорода к ее равновесной величине в жилкой фазе от удельного съема ГПК. [15] |
Страницы: 1 2