Процесс - окисление - фенол
Cтраница 1
Процесс окисления фенолов, идущий с поглощением кисло ] да, протекает неравномерно. Естественно, и подача возд в аэрационный бассейн также осуществляется неравномерно: бо шее его количество подается в начало бассейна, где особер высока скорость окисления фенолов. [1]
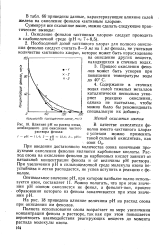 |
Влияние рН на расход озона. [2] |
Процесс окисления фенолов может быть ускорен при повышении температуры воды до 40 С. [3]
В процессе окисления орто-замещенных фенолов заместители проявляют в основном электронные эффекты ( индуктивные и резонансные), а ролью стеричвских факторов можно пренебречь. [4]
В процессе окисления орто-замещенных фенолов заместители проявляют в основном электронные эффекты ( индуктивные и резонансные), а ролью стерических факторов можно пренебречь. [5]
Однако для процесса окисления фенола, который имеет д 6, применение в 2 раза меньшей концентрации означает, что это время увеличится в 26 64 раза. [6]
В ряде случаев процесс окисления фенола оказывается весьма сложным, протекающим с образованием радикалов. В этих случаях первой стадией является образование стабилизированного резонансом феноксшгыюго радикала. [7]
Повышение температуры также значительно ускоряет процесс окисления фенолов активным хлором. Однако повышать температуру выше 45 не следует, так как при этом гипохлориты переходят в хлораты, которые обладают меньшей окислительной способностью и замедляют реакцию окисления. Оптимальной температурой окисления является 40 С. При этой температуре скорость реакции увеличивается в 2 - 3 раза по сравнению со скоростью реакции при комнатной температуре. [8]
В конечном счете при всех гемолитических процессах окисления фенолов и ароматических аминов образуется сложная смесь. [9]
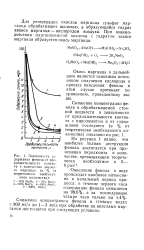 |
Зависимость содержания фенола от продолжительности контакта и количества двуокиси марганца ( в % от теоретически необходимого количества. [10] |
Окись марганца в дальнейшем является основным источником получения кислорода и процесс окисления фенола в этом случае протекает по уравнению, приведенному выше. [11]
К этому же типу реакций относится открытие Си11 по каталитическому ускорению процесса окисления фенолов ( тимола, резорцина, гидрохинона) и n - фенетидина перекисью водорода. [12]
О характере образующихся при реакции ( 16) продуктов можно делать определенные выводы по данным, полученным при изучении процесса окисления фенолов. [13]
Необходимо отметить, что если баланс по цианистому водороду и сероводороду, определенный по воде и газовой фазе, сходится удовлетворительно, то количество фенолов в воздухе после градирни значительно меньше, чем в воде, что свидетельствует о процессах окисления фенолов, происходящих на градирне. [14]
 |
Кинетика окисления фенола пероксидом водорода. [15] |
Страницы: 1 2