Процесс - медленное окисление
Cтраница 3
Механизм этого окисления был разработан А. Н. Бахом еще в начале 1897 г. в его труде О роли перекисей в процессах медленного окисления. Энергия, необходимая для активации кислорода в процессе медленного окисления, не получается извне, а доставляется самим окисляемым веществом. Поэтому при обычных температурных условиях молекулярным кислородом могут окисляться лишь химически ненасыщенные, аутоксидабель-ные вещества, тогда как насыщенные остаются без изменения. Аутоксида-бельные вещества, приходя в соприкосновение с кислородом, не расщепляют его молекулу на свободные атомы ( как это думали раньше), а превращают эту молекулу в радикал, где только одна связь является разорванной. Указанный радикал и присоединяется к окисляемому веществу. При этом неизбежно должны образовываться перекиси, которые, являясь весьма неустойчивыми и химически активными веществами, способствуют дальнейшему окислению. [31]
Пробы сыпучих материалов ( веществ, смесей), отбираемые для исследования, могут выделять токсичные вещества, что связано с происходящими в них процессами медленного окисления или разложения. Поэтому пробы должны быть упакованы в прочную и герметичную тару и снабжены паспортом с подробными данными о химическом составе и токсичности. В паспорте должны быть также указаны физические константы и другие сведения, требуемые условиями техники безопасности. Паспорт должен находиться внутри тары, а снаружи несмываемыми чернилами должно быть написано название продукта и должны быть указаны основные его свойства. Кроме того, на таре делаются предупредительные надписи, предусмотренные техникой безопасности. Пробы необходимо хранить и перевозить при пониженных температурах, поскольку с повышением температуры экзотермические процессы интенсифицируются. [32]
Перекисная теория возникла на основе учения об окислительных явлениях и была сформулирована почти одновременно и независимо друг от друга академиком А. Н. Бахом [2], проводившим исследования процессов медленного окисления в животных и растительных организмах, и К. [33]
Наши опыты по изучению реакции атомарного кислорода с простейшими углеводородами и альдегидами снимают псе экспериментальные обоснования, служившие поводом к пренебрежению роли атомарного кислорода в процессах медленного окисления. [34]
Как будет показано дальше, изучение процессов медленного окисления привело меня к заключению, что активирование кислорода может происходить при посредстве перекисей, которые являются постоянным фактором всякого процесса медленного окисления, какова бы пи была природа окисляющегося тела. [35]
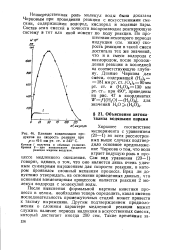 |
Влияние конденсации продуктов на скорость реакции при / 7 416 мм рт. ст. и 543 С. [36] |
Хорошее соответствие эксперимента с уравнением ( 20 - 1) во всех рассмотренных выше случаях подтвердило основное предположение Чиркова о том, что вода играет ведущую роль в процессе медленного окисления. Сам вид уравнения ( 20 - 1) говорит, однако, о том, что оно является лишь очень удачным суммарным выражением для скорости реакции, в котором проявился сложный механизм процесса. Вряд ли допустимо утверждать, на основании приведенных данных, что основным элементарным процессом является реакция 2 молекул водорода с молекулой воды. [37]
Придя к заключению, что образование перекисей может служить источником активного кислорода в организме, я раньше всего постарался уяснить себе, насколько это образование перекисей является постоянным фактором во всяком процессе медленного окисления. [38]
Не удивительно, что перекись водорода содержится в атмосфере и ее содержание в ней особенно повышается в летние месяцы, когда благодаря деятельности растительного покрова накопляются в изобилии легко окисляющиеся вещества и усиливаются процессы медленного окисления. По крайней мере часть атмосферной перекиси водорода, как доказал А. Н. Бах при помощи найденной им реакции на ШОг, получается непосредственно в ассимиляционных органах растений. Однако применение общей теории Баха к разъяснению ведущих химических процессов органического мира - ассимиляции и дыхания - выходит за рамки учебника неорганической химии. [39]
Горение материала складывается в основном из двух процессов: пламенного горения, при котором происходит экзотермическое окисление горючих газов, выделяющихся при разложении материала под влиянием нагрева, и тления, представляющего собой процесс медленного окисления угольного остатка. К антипирену, как правило, предъявляется требование тормозить тот и другой процесс. [40]
Неудивительно, что перекись водорода содержится в атмосфере и ее содержание в ней особенно повышается в летние месяцы, когда, благодаря деятельности растительного покрова, накопляются в изобилии легко окисляющиеся вещества и усиливаются процессы медленного окисления. По крайней мере часть атмосферной перекиси водорода, как доказал А. Н. Бах, при помощи найденной им реакции на Н2О2 полулается непосредственно в ассимиляционных органах растений. Однако применение общей теории Баха к разъяснению ведущих процессов органического мира - ассимиляции и дыхания - выходит за рамки учебника неорганической химии. [41]
Революционер-народоволец, он был исключен из Киевского университета и в 1885 г. эмигрировал в Швейцарию, где и вел исследования в небольшой, устроенной им лаборатории. Научные работы А. Н. Баха посвящены процессам медленного окисления. [42]
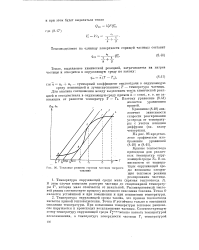 |
Тепловые режимы горения частицы твердого топлива. [43] |
В этом случае возможен разогрев частицы до стационарной температуры Т, которая мало отличается от начальной. Рассматриваемый тепловой режим соответствует процессу медленного окисления топлива. Точка О является устойчивой и при повышении и при понижении температуры. [44]
Этот метод применим при работе с неизвестным инициатором, либо в среде, где неизвестен выход радикалов в объем на одну молекулу распавшегося инициатора. Такой же метод можно применять в процессах медленного окисления, когда источник инициирования вообще неизвестен. Единственным требованием к системе в этом случае является неизменность скорости инициирования как в отдельном опыте, так и от опыта к опыту. При помощи выражения (VI.32) были определены скорость инициирования и выход радикалов на один акт распада АИБН в 2 2 4-триметилпентане. [45]
Страницы: 1 2 3 4