Процесс - оксихлорирование
Cтраница 1
 |
Зависимость результатов процесса оксихлорирования 1 2-дихлорэтана от используемого носителя. [1] |
Процесс оксихлорирования является высокоэкзотермичным, поэтому его в основном проводят в реакторах с псевдоожижен-ным слоем контакта. Для облегчения контроля за температурой часть жидкого конденсата продуктов возвращают в верхнюю часть реактора. [2]
Процесс оксихлорирования осуществляется в реакторе 5 под давлением 0 5 МПа и при температуре 200 - 280 С. Катализатор в нем находится в псевдоожиженном слое. Способ смешения и соотношение компонентов должны быть таковыми, чтобы не образовывались взрывоопасные смеси. [3]
Процесс оксихлорирования можно проводить в кожухотруб-ных аппаратах с созданием в трубках множества кипящих слоев катализатора. Тепло реакции снимается кипящим теплоносителем ( например, водой), пары которого, конденсируясь в специальном холодильнике, стекают обратно в аппарат. Диаметр трубок с катализатором должен быть не более 380 мм. [4]
Процесс оксихлорирования проводят в широком интервале температур ( 300 - 600 С), времени контакта ( 4 - 30 с) в присутствии катализатора, содержащего соли металлов переменной валентности. В качестве исходного углеводородного сырья используют, как правило, полихлориды С2 разного состава. Источником кислорода в процессе оксихлорирования может быть концентрированный кислород, воздух или другой кислородсодержащий газ. Обычно в качестве хлорирующего агента используют хлорид водорода, но возможно использование хлора. [5]
Процесс оксихлорирования этилена в неподвижном слое катализатора обычно является многостадийным. Это облегчает управление сильноэкзотермической реакцией. На рис. 3 показана схема трехстадийной установки оксихлорирования с реактором для извлечения этилена. Реакторы соединены друг с другом последовательно, в каждый реактор подают воздух. По конструкции реакторы подобны большим трубчатым теплообменникам ( рис. 4) и содержат много узких вертикальных трубок, вваренных сверху и снизу в трубные решетки. Внутрь трубок диаметром около 25 мм помещают катализатор. Диаметр трубок выбирают с таким расчетом, чтобы температура реакции не превышала температуру, при которой возможно разрушение катализатора. В трубках большего диаметра теплопередача от центра трубки к ее стенкам замедлена, и катализатор разогревается до более высоких температур. [6]
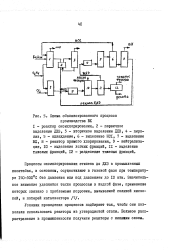 |
Схема сбалансированного процесса. [7] |
Процессы оксихлорирования этилена до ДХЭ в промышленных масштабах, в основном, осуществляют в газовой фазе при температуре 150 - 300 С без давления или под давлением до 10 атм. [8]
Процессы оксихлорирования бензола предназначены, в основном, для получения монохлорбензола в производстве фенола. [9]
Процесс оксихлорирования этилена в неподвижном слое катализатора обычно является многостадийным. Это облегчает управление сильноэкзотермической реакцией. На рис. 3 показана схема трехстадийной установки оксихлорирования с реактором для извлечения этилена. Реакторы соединены друг с другом последовательно, в каждый реактор подают воздух. По конструкции реакторы подобны большим трубчатым теплообменникам ( рис. 4) и содержат много узких вертикальных трубок, вваренных сверху и снизу в трубные решетки. Внутрь трубок диаметром около 25 мм помещают катализатор. Диаметр трубок выбирают с таким расчетом, чтобы температура реакции не превышала температуру, при которой возможно разрушение катализатора. В трубках большего диаметра теплопередача от центра трубки к ее стенкам замедлена, и катализатор разогревается до более высоких температур. [10]
Процесс жидкофазного оксихлорирования этилена имеет ряд преимуществ перед каталитическим газофазным оксихлорированием. [11]
Суммарно процесс оксихлорирования, например, этилена до дихлорэтана ( ДХЭ) сводится к следующему уравнению: 2НСМ / 202 i - CoH - - CoH CIp HoO. Реакция идет в присутствии катализатора Дикона. [12]
Реагентами процессов оксихлорирования могут - быть насыщенные ( метан, этан, пропан), ненасыщенные ( этилен, пропилен) и ароматические ( бензол) углеводороды или их хлорпроизводные. [13]
Внедрение процесса оксихлорирования в хлорорганическом синтезе обеспечиваем потребление значительных количеств абгазного хлористого водорода и снижает себестоимость производства конечных продуктов. [14]
Селективность процесса оксихлорирования зависит от катализатора, от связи Ме-CI, и от пористости носителя. [15]
Страницы: 1 2 3 4