Процесс - распад - молекула
Cтраница 2
К а р л и н и др. Радиационная стойкость полидиметилсилоксанов, содержащих группы метилфенил - или дифенилсилоксанов в процессе распада молекул на радикалы. [16]
Мерой физической устойчивости многоатомной молекулы служит энергия диссоциации или энергия: атомизации молекулы Л - изменение-энергии в идеальном газовом состоянии для процесса распада молекулы на атомы при О. [17]
Как видно из табл. 33, различие в значениях ДО ИОниэ а следовательно, и р / Сиониз определяется в наибольшей степени ДО0 процесса распада молекул HHal на атомы. [18]
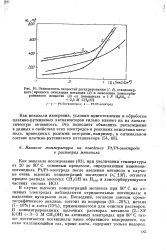 |
Зависимость скоростей дегидрирования ( 1, 4, стационарного процесса окисления метанола ( 2 и окисления хемосорби-рованного вещества ( 3 от потенциала в 1 N H2SO4. [19] |
Как показало исследование [83], при увеличении температуры от 20 до 80 С основным процессом, определяющим изменение потенциала Pt / Pt-электрода после введения метанола в случае не очень высоких концентраций последнего ( 1 - М), остается процесс распада молекул СН3ОН на Надс и хемосорбирующуюся частицу состава НСО. [20]
Изучение превращений [ 3-тетралилдецилсульфида представляло интерес в том отношении, что тетралиновое ядро является конденсированной системой бензольного и гексаметиленового циклов, и хотя сера в этом сульфиде непосредственно связана с бензольным циклом, не исключалась возможность влияния и гексаметиленового кольца на процесс распада молекулы. [21]
Это означает, что его электрический заряд равен одной отрицательной единице. Процесс распада молекул на ионы называется электролитической диссоциацией. Неэлектролитами являются растворенные газы и различные органические вещества. [22]
Молекулы солей, кислот и оснований при растворении их в воде или других растворителях распадаются - диссоциируют на электрически заряженные ( положительно или отрицательно) частицы, называемые ионами. Процесс распада молекул растворенных веществ на ионы под влиянием молекул растворителя называется электролитической диссоциацией, а вещества, диссоциирующие в растворе - электролитами. [23]
В 1922 г. Линденман предложил схему, позволяющую понять механизм мономолекулярных реакций, исходя из представлений о столкновении молекул. Чтобы произошел мономолекулярный процесс распада молекулы А, необходимо, чтобы она обладала колебательной энергией, достаточной для разрыва связей. [24]
Плотность дистиллята от коксования гудрона по мере повышения температуры в кубе также непрерывно возрастает. По-видимому, процессу распада молекул сырья на более мелкие осколки в случае гудронов предшествует ( при 365 - 385 С) процесс деполимеризации высокополимерных сильно разветвленных естественных углеводородных комплексов нефтей с длинными алифатическими цепями на комплексы меньших молекулярных размеров. [25]
В основе биотрансформации токсичных веществ лежит несколько типов химических реакций, в результате которых происходит присоединение или же отщепление метиль-ных ( - СН3), ацетильных ( СН3СОО -), карбоксильных ( - СООН), гидроксильных ( - ОН) радикалов ( групп), а также атомов серы и серосодержащих группировок. Немалое значение имеют процессы распада молекул ядов вплоть до необратимой трансформации их циклических радикалов. Но особую роль среди механизмов обезвреживания ядов играют реакции синтеза, или конъюгации, в результате которых образуются нетоксичные комплексы - конъюгаты. [26]
Все вышесказанное относится как к реакциям в газовой фазе, так и к реакциям в жидкой фазе, однако в последнем случае появляются некоторые дополнительные особенности. Наличие растворителя затрудняет процесс распада молекул растворенного вещества на радикалы. [27]
Все вышесказанное относится как к реакциям в газовой фазе, так и к реакциям в жидкой фазе, однако в последнем случае появляются некоторые дополнительные особенности. Наличие растворителя затрудняет процесс распада молекул растворенного вещества на радикалы. Это связано с тем, что образующиеся радикалы в большинстве случаев с трудом могут отойти друг от друга из-за малого значения коэффициента диффузии в жидкостях и поэтому тут же вновь рекомбшшруют. Радикалы как бы заключены в клетку из окружающих их молекул растворителя. Если же все-таки радикалам удается разойтись, то оказывается весьма затрудненным процесс их рекомбинации. Поэтому при реакциях в жидкой фазе диссоциация на радикалы и их рекомбинация протекают с другими скоростями, чем в газовой фазе. Поскольку при этом уменьшаются скорости обоих процессов, стационарная концентрация радикалов существенно не изменяется. [28]
В 1922 г. Линдеман дал схему, позволяющую понять механизм мономолекулярных реакций, исходя из представлений о столкновении молекул. Для того чтобы произошел мономолекулярный процесс распада молекулы А, ей необходимо обладать достаточной колебательной энергией для разрыва связей. [29]
Молекула бромистого водорода значительно менее прочна, чем молекула хлористого водорода. При синтезе бромистого водорода одновременно идет процесс частичного распада молекул на элементы. Следовательно, реакция образования бромистого водорода является реакцией обратимой. [30]
Страницы: 1 2 3