Процесс - взаимодействие - углерод
Cтраница 1
Процесс взаимодействия углерода с газообразными реагентами протекает как на внешней ( контурной), так и на внутренней поверхности макро - и микршор, доступных молекулам газообразного реагента. [1]
 |
Разность энтальпий реакций раскисления. [2] |
Процесс взаимодействия углерода с окисленным железом ( кипение при плавке стали) является очень важным, однако единого мнения по этому вопросу еще не сложилось до сих пор. [3]
Экспериментально процесс взаимодействия углерода с водяным паром и двуокисью углерода с целью определения кинетических характеристик изучен в проточном реакторе. В отличие от реакций в замкнутом объеме, реакции в потоке проводятся в стационарных условиях. [4]
Условно по характеру процессов взаимодействия углерода топлива с кислородом дутья вагранка может быть разделена на четыре зоны. Процессы, происходящие в отдельных зонах вагранки, следующие. [5]
Основным итогом химической стороны процесса взаимодействия углерода с кислородом при высоких температурах является соединение кислорода с углеродом по реакциям С 02 С02 и 2С О2 2СО, эти реакции принято называть первичными. [6]
Вывод о том, что при высоких температурах процесс взаимодействия углерода с СО определяется равновесной концентрацией кислорода, вполне естествен, так как условие a - К. Что же касается второго вывода о том, что при достаточно низких температурах ( кинетический режим для реакции С О2) процесс взаимодействия углерода с СО2 в основном определяется равновесной концентрацией кислорода, то он является в некоторой степени неожиданным. [7]
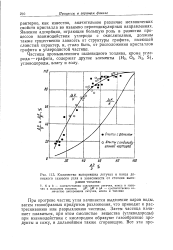 |
Количество выгоревших летучих и кокса донецкого газового угля в зависимости от степени выгорания топлива. [8] |
Явления адсорбции, играющие большую роль в развитии процессов взаимодействия углерода с окислителями, должны также существенно зависеть от структуры графита, имеющей слоистый характер, и, стало быть, от расположения кристаллов графита в углеродистой частице. [9]
В зависимости от температуры, парциального давления и других условий процесс взаимодействия углерода с газами определяется разными стадиями, и скорость реакции, определяемая по уравнениям ( XV-4), ( XV-5), ( XV-6), может иметь различную зависимость от концентрации и температуры газового реагента. Из анализа этих уравнений следует, что реакция может иметь любой порядок от 0 до 1, а также довольно различные кажущиеся энергии активации, так как каждая стадия имеет свою энергию активации. [10]
Скорость газового потока сильно влияет на скорость диффузии, определяющей во времени процесс взаимодействия углерода с кислородом. [11]
Так, при горении и газификации в газогенераторах при температурах 1000 - 1100 С процесс взаимодействия углерода с кислородом протекает в диффузионной области, а при этих же условиях реакция восстановления углекислоты находится в кинетической области реагирования. [12]
Горение и газификация твердых топлив рассматриваются как единый неразрывный процесс с точки зрения общности химических реакций и ведущей роли процесса взаимодействия углерода с кислородом дутья. [13]
В связи с более высокой энергией активации реакции ( 1) по сравнению с энергией активации ( 2) при температурах 1000 С процесс взаимодействия углерода с кислородом протекает в диффузионной области, а реакции ( 1) - в области реагирования, близкой к кинетической. [14]
В более поздних работах Баддур и Йвасек [4] и Баддур и Бланше [5] показали, что не только радикал С3Н, но также и радикалы С3Н, С4Н, СН н СН2 должны присутствовать в системе для того, чтобы можно было объяснить величины выходов ацетилена, полученных в процессе взаимодействия углерода с водородом в высокотемпературной дуге. [15]
Страницы: 1 2