Процесс - восстановление - никель
Cтраница 1
Процесс восстановления никеля протекает только на поверхности металлов, способных каталитически влиять на эту реакцию. К числу таких металлов относятся палладий, никель, железо, алюминий и некоторые другие. Покрытия на меди и ее сплавах могут быть получены только в случае контакта их в начале процесса с более § электроотрицательным металлом - железом, алюминием или никелем. В дальнейшем роль катализатора выполняет осаждающийся никель. На некоторых металлах, например свинце, кадмии, олове и др., вообще не удается получить никелевого покрытия. [1]
На процесс восстановления никеля определенное влияние оказывает площадь покрываемой поверхности. Время, необходимое для выделения одного и того же количества металла, обратно пропорционально площади загружаемой поверхности. [2]
Для процессов восстановления никеля, например, характерны повышенные температуры ( почти до 100 С в кислых растворах), а для процесса химического восстановления меди формальдегидом - температуры 20 - 50 С, причем выбор температурного режима определяется природой лиганда. Химическое меднение в тартратных растворах проводят обычно при температуре от 18 до 30 С, а в растворах на основе ЭДТА - при температуре выше 40 С. Стабильность растворов химического меднения с повышением температуры снижается, поэтому в растворах, работающих при повышенных температурах, всегда содержатся стабилизирующие добавки, которые позволяют получать осадки хорошего качества даже при температурах, более 70 С. [3]
Скорость процесса восстановления никеля зависит прежде всего от температуры и кислотности раствора. При низкой температуре процесс практически не идет. Температура раствора должна быть от 80 до 98 С. [4]
Для процессов восстановления никеля, например, характерны повышенные температуры ( почти до 100 С в кислых растворах), а для процесса химического восстановления меди формальдегидом - температуры 20 - 50 С, причем выбор температурного режима определяется природой лиганда. Химическое меднение в тартратных растворах проводят обычно при температуре от 18 до 30 С, а в растворах на основе ЭДТА - при температуре выше 40 С. Стабильность растворов химического меднения с повышением температуры снижается, поэтому в растворах, работающих при повышенных температурах, всегда содержатся стабилизирующие добавки, которые позволяют получать осадки хорошего качества даже при температурах, более 70 С. [5]
Для процессов восстановления никеля, например, характерны повышенные температуры ( почти до 100 С в кислых растворах), а для процесса химического восстановления меди формальдегидом - температуры 20 - 50 С, причем выбор температурного режима определяется природой лиганда. Химическое меднение в тартратных растворах проводят обычно при температуре от 18 до 30 С, а в растворах на основе ЭДТА - при температуре выше 40 С. Стабильность растворов химического меднения с повышением температуры снижается, поэтому в растворах, работающих при повышенных температурах, всегда содержатся стабилизирующие добавки, которые позволяют получать осадки хорошего качества даже при температурах, более 70 СС. [6]
Органические добавки ускоряют процесс восстановления никеля; некоторые из них связывают ионы никеля в комплексное соединение, предупреждая выпадение фосфитов никеля. Скорость восстановления никеля возрастает до максимума с увеличением концентрации добавок, при - этом осаждаются гладкие, блестящие осадки. При дальнейшем повышении концентрации органических соединений скорость осаждения никеля падает, качество осадков ухудшается. [7]
Если считать, что процесс восстановления никеля контролируется стадией разложения гипофосфита, то лучше всего объясняет роль органических добавок предположение Гутцей-та [384], согласно которому добавки ускоряют разложение гипофосфита вследствие ослабления связи водородного атома с атомом фосфора. Эта гипотеза хорошо объясняет взаимную зависимость скорости выделения никеля и атомарного водорода от концентрации гипофосфита и органических добавок. [8]
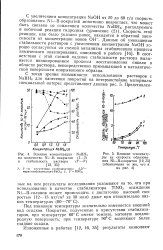 |
Влияние температуры на скорость образования Ni - В-покрытия ( обозначения те же, что и на 4. [9] |
В соответствии с этой схемой падение стабильности раствора вызывается инициированием процесса восстановления никеля в области раствора, непосредственно примыкающей к каталитической поверхности покрываемого образца. [10]
Специальной подготовки при этом е требуется, так как алюминий катализирует процесс восстановления никеля из его растворов. Покрытие получается равномерным по всей конфигурации поверхности. [11]
Фосфор образует интерметаллическое соединение с никелем. Реакцией, определяющей скорость процесса восстановления никеля, является разложение гипофосфита с образованием атомарного водорода. Разложение гипофосфита ускоряется с повышением температуры и увеличением концентрации гипофосфита и при введении некоторых органических кислот. При отсутствии катализаторов гипофосфит может разлагаться лишь в щелочной среде. Работы с изотопами показали, что выделяющийся атомарный водород может отщепляться из групп ОН -, а также из групп, связанных непосредственно с фосфором. Как видно, факторы, определяющие скорость разложения гипофосфита, определяют и скорость осаждения никеля. [12]
Восстановление никелевых солей с помощью гипофосфита протекает толькояа некоторых металлах, относящихся к VIII группе периодической системы элементов, способных катализировать процесс. Примеси солей свинца и кадмия полностью прекращают процесс восстановления никеля. [13]
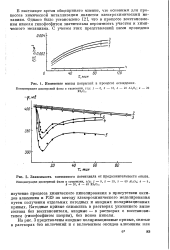 |
Изменение массы покрытий в процессе осаждения.| Зависимость смешанного потенциала от продолжительности опыта. [14] |
В настоящее время общепринято мнение, что основным для процессов химической металлизации является электрохимический механизм. Однако было установлено [2], что в процессе восстановления никеля гипофосфитом значительна вероятность участия и химического механизма. [15]
Страницы: 1 2