Процесс - катодное восстановление
Cтраница 3
За счет растворения восстановленной фазы обнажаются свежие слои, более богатые ионами Ni3, на которых снова начинает протекать процесс катодного восстановления с образованием окисла нового состава. [31]
В сильнокислых перхлоратных растворах, так же как в других растворах в отсутствие активирующих анионов и комплексо-о бразования, процесс катодного восстановления индия на ртути настолько необратим, что отвечающая ему катодная волна появляется на полярограмме лишь в области потенциалов от - 0 9 до - 1 0 в ( насыщ. [32]
 |
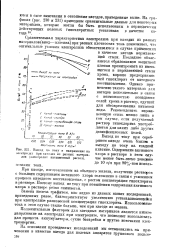
Влияние температуры на износ графитовых анодов. [33] |
При введении небольшого количества хроматов выход хлората по току сильно возрастает, так как в этих условиях снижается скорость процессов катодного восстановления гипохлорита. [34]
 |
Выход по току и напряжение на электродах при катодах из разных материалов ( электролит насыщенный рассол. [35] |
При катоде, изготовленном из обычного железа, получение растворов с большим содержанием активного хлора осложнено в связи с усилением процесса катодного восстановления, с ростом концентрации гипохлорита в растворе. Поэтому выход по току при повышении содержания активного хлора в растворе резко снижается. [36]
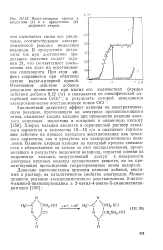 |
Вольт-амперные кривые в. [37] |
Хлорид кальция вводится в сернокислый раствор исходного наркотина в количестве 10 - 15 г / л и оказывает тормозящее действие на процесс катодного восстановления как исходного наркотина, так и продуктов его электрохимического окисления. Влияние хлорида кальция на катодный процесс связывается с образованием на катоде за счет подщелачивания, происходящего в результате выделения водорода, пористой пленки из гидроксида кальция, затрудняющей доступ к поверхности электрода крупных молекул органических веществ, но не препятствующих прохождению гидратированных ионов водорода. [38]
Помимо потери электродных продуктов за счет электрохимических процессов, в электролизере непосредственно взаимодействуют электродные продукты или идут аналогичные им по результатам процессы катодного восстановления. Это также вызывает потери. Интенсивностью процессов не может быть обнаружена объективными методами и определяется по разности. [39]
Поляризационная кривая электрода, содержащего активированный уголь БАУ с нанесенным полифталоцианином кобальта - железа, лежит ниже поляризационной кривой платины и выше поляризационной кривой чистого носителя в процессе катодного восстановления кислорода. [40]
Удаление кислорода из раствора, с одной стороны, затормаживает катодный процесс пассивации вследствие уменьшения скорости катодного восстановления кислорода, а с другой-увеличивает катодную плотность тока, связанную с увеличением скорости процесса катодного восстановления молекул воды. Из этой кривой видно, что участок ав подчиняется логарифмической зависимости. В этой области, как и в предыдущем случае ( рис. 1), происходит катодное восстановление молекул воды с образованием молекул водорода. В области потенциалов, соответствующих участку ее, плотность поляризующего тока остается постоянной и все еще находится в катодной области поляризации. Это свидетельствует о торможении таких процессов, как катодное восстановление молекул воды. [41]
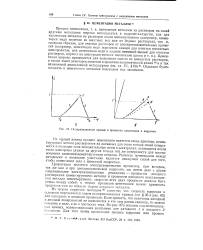 |
Поляризационные кривые в процессах цементации и коррозии. [42] |
Цементация является электрохимическим процессом, при котором, так же как и при электрохимической коррозии, мы имеем дело с двумя сопряженными электрохимическими реакциями - процессом анодного растворения цементирующего металла и процессом катодного восстановления металла цементируемого: скорости этих двух процессов должны быть равны между собой; к теории процессов цементации можно применить представления из области теории коррозии металлов. [43]
Несмотря на то что электролиты фона играют решающею роль в препаративной электрохимии, об этих инертных помощниках известно пока немного, В принципе, в условиях эчектро-химнчсских реакций можно применять любые катионы и анионы Для процессов катодного восстановления наиболее подходящими являются соли щелочных металлов н ониевые соли, особенно четвертичные аммониевые соли, пригодны также фосфо-ниевые, арсонпевыс и сульфопиевые соли. Однако нужно отметить, что ониевые соли могут при восстановлении разлагаться, если потенциалы их разряда более положительны, чем потенциал восстановления исследуемого вещества Химические реакции, связанные с разрядом оииевых катионов, рассмотрены в гл. [44]
Зависимость напряжения на электролизере и потерь выхода nov току от межэлектродного расстояния при различных плотностях тока была объектом тщательного изучения [38]: При увеличении платности тока можно уменьшить межэлектродное расстояние до определенного предела без того, чтобы при этом заметно не снизился, выход по току из-за процессов катодного восстановления активного хлора. При применении вертикальных или очень наклонных катодов процессы катодного восстановления могут сильно возрастать, так как на поверхности раздела амальгамы и раствора электролита возникает интенсивная турбулизация потока. [45]
Страницы: 1 2 3 4