Процесс - катодная деполяризация
Cтраница 1
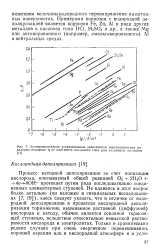 |
Экспериментально установленные зависимости перенапряжения выделения водорода 11 от плотности катодного тока для различных металлов. [1] |
Процесс катодной деполяризации за счет ионизации кислорода, описываемый общей реакцией Ог 2Н2О 4е - - 4ОН - протекает путем ряда последовательно соединенных элементарных ступеней. Не вдаваясь в этот вопрос более детально ( он изложен в специальных исследованиях [7, 19]), здесь следует указать, что в отличие от водородной деполяризации в процессах кислородной деполяризации торможение, вызываемое доставкой ( диффузией) кислорода к катоду, обычно является основной тормозящей ступенью, вследствие относительно невысокой растворимости кислорода в электролитах. [2]
Процесс катодной деполяризации с ионами Fe3 или с щелочным раствором нитрата калия протекает беспрепятственно до образования иона Fe2 или аммиака. Ионы металлов более благородных, чем цинк, вызывают растворение через обмен; при этом они восстанавливаются до металлического состояния. [3]
Процесс катодной деполяризации железа, стали и алюминия под действием сульфатредуцирующих бактерий можно исследовать экспериментально методом снятия поляризационных кривых, характер которых позволяет судить об интенсивности коррозионного процесса, обусловленного жизнедеятельностью бактерий. При изучении процесса катодной деполяризации с использованием как гидрогеназ-положительных, так и гидрогеназ-отрицательных сульфатредуцирующих бактерий было установлено, что скорость коррозии металла зависит от содержания железа в среде. [4]
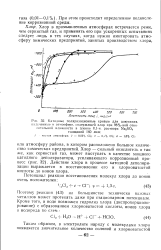 |
Катодные поляризационные кривые для алюминия, полученные и атмосфере, содержащей хлор при 98 % - ной относительной влажности в пленке 0 1 - н. раствора N32804 толщиной 160 мкм. [5] |
Действие хлора в процессе катодной деполяризации выражается в восстановлении его и хлорноватистой кислоты до ионов хлора. [6]
О влиянии сульфида железа на процесс катодной деполяризации свидетельствует стабилизация во времени стационарного потенциала углеродистой стали, что с учетом роста скорости коррозии и облегчения анодного процесса в присутствии сероводорода может быть объяснено только облегчением катодного процесса. [7]
В настоящее время наиболее полно изучен процесс катодной деполяризации лишь под действием основных коррозионных агентов: кислорода и ионов водорода. [8]
В настоящее время наиболее полно изучен процесс катодной деполяризации лишь под действием основных коррозионных агентов-кислорода и ионов водорода. [9]
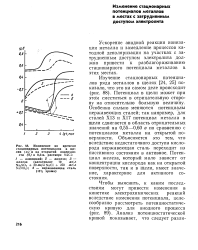 |
Изменение во времени стационарных потенциалов в щс - ( а и на открытой поверхно - ( б в 0 5. [10] |
Ускорение анодной реакции ионизации металла и замедление процессов катодной деполяризации на участках с затрудненным доступом электролита должно привести к разблагораживанию стационарного потенциала металлов в этих местах. [11]
Что же касается нейтральных электролитов, в которых процесс катодной деполяризации совершается за счет диффузии кислорода к поверхности, являющейся часто неравномерной, то в них коррозия, как правило, носит локальный характер даже в хорошо проводящих ток электролитах. [12]
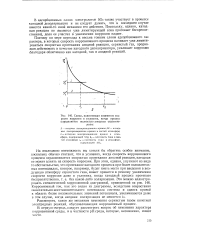 |
Схема, поясняющая изменение скорости коррозии в условиях, когда процесс определяется полностью анодным ограничением. [13] |
В адсорбционных слоях электролитов SO2 также участвует в процессе катодной деполяризации и не следует думать, что в последнем случае имеется какой-то иной механизм его действия. Поскольку, однако, катодная реакция не является уже лимитирующей ( она протекает беспрепятственно), доля ее участия в увеличении коррозии падает. [14]
Кислород, находящийся со средой в зазоре, рас ходуется в процессе катодной деполяризации. Концентрация его в зазоре при этом понижается. [15]
Страницы: 1 2 3