Процесс - катодная деполяризация
Cтраница 2
Исключение составляют случаи, когда повышение температуры уменьшает растворимость газов, участвующих в процессе катодной деполяризации, например, кислорода. По этой причине кривая зависимости скорости, коррозии железа от температуры в; открытых системах проходит через максимум ( 70 С), в закрытых же системах наблюдается непрерывное увеличение скорости коррозии с температурой. [16]
Исключение составляют случаи, когда повышение температуры уменьшает растворимость газов, участвующих в процессе катодной деполяризации, например, кислорода. [17]
Ускорение катодного процесса вызвано восстановчением нитрогрупп в молекулах нитрофенолятов аминов, т.е. их участием в процессе катодной деполяризации. [18]
В видимых слоях электролитов, в которых процесс анодного растворения большинства черных металлов протекает без заметного торможения реакции, стимулирующее действие хлора следует связывать в основном с облегчением процесса катодной деполяризации. [19]
Новые данные по электрохимической кинетике, полученные нами, ставят под сомнение правдоподобность такого механизма, и поэтому выдвигается другая точка зрения, которая действие этого газа сводит к ускорению процесса катодной деполяризации. Оказалось, что сернистый ангидрид является мощным катодным деполяризатором. Ясно, что в зависимости от того, какой принять механизм, в основу противокоррозионной защиты должны быть положены различные принципы; в первом случае следует попытаться воздействовать на реакцию окисления сернистого ангидрида до серного или повысить перенапряжение водорода, во втором же необходимо замедлить реакции восстановления сернистого ангидрида ( H2S03, HS03 -), что можно, например, достигнуть подбором соответствующего ингибитора. [20]
Тенденция к ускорению коррозии в начале испытания связана, по-видимому, с разрушением естественной окисной пленки и накоплением на поверхности образцов катодных включений сплава, которые усиливают электрохимическую неоднородность поверхности и облегчают процессы катодной деполяризации. [21]
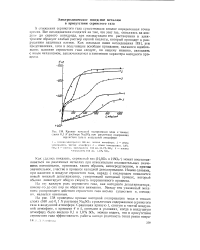 |
Кривые катодной поляризации меди е тонких. [22] |
Как удалось показать, сернистый газ ( H2SOs и HSOs) может восстанавливаться на различных металлах при относительно положительных значениях потенциалов, принимая, таким образом, непосредственное, и притом значительное, участие в процессе катодной деполяризации. Иными словами, при наличии в воздухе сернистого газа, наряду с кислородом появляется новый мощный деполяризатор, ускоряющий катодный процесс, который обычно лимитирует общую скорость коррозионного процесса. [23]
Электрохимические исследования стальных пластин - электродов, покрытых слоем дисульфида молибдена или графита, в сравнении с чистыми пластинами в камере постоянного тока ( метод ОПИ) и камере пульсирующего тока ( метод ОПС - ООС) показали, что графит и особенно дисульфид молибдена MoS2 значительно снижают общее и поляризационное сопротивление чистых металлических пластинок, усиливают коррозионный ток, качественно меняют структуру пленки на поверхности металла, не давая образовываться окионым пассивным слоям, усиливают процесс анодного растворения металла и, в меньшей степени, - процесс катодной деполяризации. Эти наполнители усиливают также процессы химической коррозии, прежде всего цветных металлов. Поэтому при диспергировании дисульфида молибдена и графита, чтобы придать им коллоидную ( агрегативную) устойчивость, целесообразно использовать ПАВ, которые одновременно с диспергированием и стабилизацией твердых частиц этих веществ в объеме ликвидируют их коррозионную агрессивность. [24]
Процесс катодной деполяризации железа, стали и алюминия под действием сульфатредуцирующих бактерий можно исследовать экспериментально методом снятия поляризационных кривых, характер которых позволяет судить об интенсивности коррозионного процесса, обусловленного жизнедеятельностью бактерий. При изучении процесса катодной деполяризации с использованием как гидрогеназ-положительных, так и гидрогеназ-отрицательных сульфатредуцирующих бактерий было установлено, что скорость коррозии металла зависит от содержания железа в среде. [25]
Процесс коррозии стали в средах с СО2 протекает с водородной деполяризацией и ускоряется вследствие повышенной растворимости продуктов коррозии и невозможности образования защитных карбонатных пленок. Исследованиями последних лет доказана гипотеза о возможности участия двуокиси углерода в процессе катодной деполяризации с восстановлением СОа до метана. [26]
Графит и особенно MoSs, введенные в неингибированные смазочные материалы, значительно снижают общее и поляризационное сопротивление металлических пластинок, усиливают коррозионный ток, качественно меняют структуру пленки на поверхности металла, не давая образовываться окисным пассивным слоям. При этом усиливается процесс анодного растворения металла и; в меньшей степени, процесс катодной деполяризации. [27]
Графит и особенно MoS2 введенные в неингибированные смазочные материалы, значительно снижают общее и поляризационное сопротивление металлических пластинок, усиливают коррозионный ток, качественно меняют структуру пленки на поверхности металла, не давая образовываться окисным пассивным слоям. При этом усиливается процесс анодного растворения металла и, в меньшей степени, процесс катодной деполяризации. [28]
При рассмотрении данных, приведенных на рис. 45, видно, что при Та, равном 10 с-1 мин, TR почти одно и то же, что объясняется кратковременностью поляризации. При длительной прерывистой поляризации на поверхности металла могут образоваться плотные катодные осадки, замедляющие процесс катодной деполяризации. [29]
В ПИНС-РК широко используют дисульфид молибдена и графит, обладающие слоистой структурой и высокими смазывающими свойствами. Исследования стальных пластин-электродов, чистых и покрытых слоем дисульфида молибдена или графита, в камере постоянного и пульсирующего токов ( метод ОПС - ООС) показывает, что графит и особенно M0S2 значительно снижают общее и поляризационное сопротивление чистых металлических пластинок, усиливают коррозионный ток, ка ест-венно меняют структуру пленки на поверхности металла, не давая образовываться оксидным пассивным слоям, усиливают процесс анодного растворения металла и ( в меньшей степени) процесс катодной деполяризации. Эти наполнители усиливают также процессы химической коррозии и прежде всего цветных металлов. [30]
Страницы: 1 2 3