Электрохимический коррозионный процесс
Cтраница 1
Электрохимические коррозионные процессы протекают в водных растворах электролитов, влажных газах, расплавленных солях и щелочах. В условиях химических производств наиболее распространена электрохимическая коррозия. [1]
Электрохимические коррозионные процессы протекают в основном в водных растворах электролитов. [2]
Исследованию взаимосвязи электрохимических коррозионных процессов с процессами трения и изнашивания материалов в буровой технологии уделяется мало внимания. [3]
Суммарная скорость электрохимического коррозионного процесса определяется скоростью наиболее заторможенной стадии. [4]
 |
Принципиальная схема работы коррозионного гальванического элемента. [5] |
Кинетические характеристики электрохимических коррозионных процессов удобно представлять графически в виде совокупности поляризационных кривых катодного и анодного процессов. По оси ординат откладывают потенциалы анодных и катодных процессов ( фа и фк), по оси абсцисс - соответствующие анодные и катодные токи. [6]
 |
Принципиальная схема работы кор-роаионного гальванического элемента. [7] |
Кинетические характеристики электрохимических коррозионных процессов удобно представлять графически в виде совокупности поляризационных кривых катодного и анодного процессов. По оси ординат откладывают потенциалы анодных и катодных процессов ( сра и срк), по оси абсцисс - соответствующие анодные и катодные токи. [8]
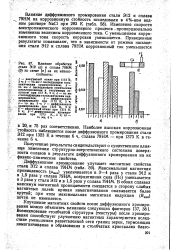 |
Влияние обработки стали Э12 ( а и сплава 79НМ ( б по схеме [ в ] на их износо - стойкость. [9] |
Изменение скорости электрохимического коррозионного процесса / пропорционально изменению величины коррозионного тока. G уменьшением коррозионного тока скорость коррозии уменьшается. [10]
Методы исследования электрохимических и коррозионных процессов при наложении переменного тока в последние годы находят все большее применение, так как они дают возможность полнее судить о кинетике различных стадий электродных реакций. [11]
Необходимым условием всякого электрохимического коррозионного процесса является неравенство Еа. Основным условием возможности прохождения процесса коррозии металла с водородной деполяризацией с определенной скоростью является требование, чтобы электродный потенциал анода ( металла) был более отрицателен, чем потенциал разряда водородных ионов с этой скоростью при данных условиях. [12]
В этом случае анализ электрохимических коррозионных процессов состоит в изучении физико-химических закономерностей отдельно катодных и анодных реакций и условий их совместного осуществления. [13]
В этом случае протекание электрохимических коррозионных процессов вследствие присутствия на поверхности металла весьма тонкого слоя электролита несколько отличается от хода электрохимической коррозии металла, погруженного и раствор электролита. Отличие состоит прежде всего в том, что тонкая пленка влаги ( электролита) является слабым препятствием для диффузии кислорода воздуха к поверхности металла. [14]
В этом случае анализ электрохимических коррозионных процессов состоит в изучении физико-химических закономерностей отдельно катодных и анодных реакций и условий их совместного осуществления. [15]
Страницы: 1 2 3 4