Введение - щелочь
Cтраница 1
Введение щелочей ускоряет растворенье шлеко-пого стекла, имеющего кислый характер. При добавке гипсе, наблюдается сульфатная активация образуются гвдросульфоалюминаты различной основности ускоряющие структурообразование. [1]
После введения щелочи суспензию перемешивали т: течение 20 мин; затем часть ее отбирали на анализ. В жидкой фазе определяли рЫ при помощи рН - метра ЛПУ-01; величины [ S2 - ] и [ Са 2 ] определяли количественно; присутствие ионов Fe2 и Fe3 оценивали качественно. [2]
При введении щелочи на верхние тарелки ректификационной колонны для их омыления образуются соли жирных кислот. Эти соли попадают в ректификат. При разбавлении спирта водой они, по мнению авторов исследований, придают ему горький вкус и неприятный запах. [3]
При введении щелочи в раствор сильной кислоты рН раствора в начале нейтрализации почти не изменяется. Тем не менее раствор сильной кислоты ( как и щелочи) не называют буферным. [4]
При введении щелочи в водные растворы солей ртути ( П) выпадает осадок оксида ртути ( П) HgO. Катионы диртути ( 2) в щелочной среде подвергаются дисмутации с выделением металлической ртути и HgO. Гидроксиды ртути ( 1) и ( II), а также оксид ртути ( 1) неизвестны. Аналогичный эффект наблюдается при введении в растворы солей диртути ( 2) сероводорода: выделяются HgS и Hg, поскольку сульфид состава Hg2S неизвестен. Малорастворимый HgS встречается в природе - это минерал киноварь. Соединения ртути ( 1) проявляют и восстановительные, и окислительные свойства. [5]
 |
Зависимость отношения Mo / Fe в осадках ферроцианидов молибдена от рН среды.| Изменение состава осадка в системе Н2Мо04 - Li4 [ Fe ( CN ei - Н20 - ( СН3 2СО. [6] |
Напротив, введение щелочи способствует связыванию ионов водорода, сдвигая тем самым равновесие в сторону конденсации ионов молибденила с образованием изополикатионов. В интервале 1 9 рН С 5 осаждается нормальный ферроцианид молибденила ( Мо02) г [ Ре ( СМ) 6 ], что свидетельствует об устойчивости Мо02 при этой кислотности. [7]
Это достигается введением щелочи или буферного раствора. [8]
Успешному протеканию реакции способствовало введение щелочи, количество которой немного превышало необходимое для нейтрализации выделявшейся кислоты. [9]
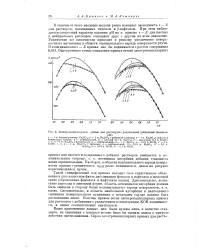 |
Электрокаиилляриые кривые для растворов с различными добавками ( влияние. [10] |
В отличие от этого введение щелочи резко изменяет зависимость а - Е для растворов, насыщенных тимолом и [ 3-нафтолом. При этом наблюдается следующий характер влияния рН на а: кривые а - Е для кислых и нейтральных растворов совпадают друг с другом во всем диапазоне. Увеличение же щелочности приводит к резкому увеличению поверхностного натяжения в области отрицательного заряда поверхности ртути. В этом диапазоне о - Е кривая как бы поднимается с ростом содержания КОН. [11]
 |
Потери при прокаливании, %, при гидратации C2S в водной и щелочной среде. [12] |
Из табл. 22 следует, что введение щелочи несколько увеличивает степень гидратации ( а) на самой первой стадии ( см. кинетическую кривую гидратации на рис. 46), но на второй стадии индукционный период в присутствии щелочи растягивается для P - C2S более чем в два раза, что свидетельствует о блокирующем действии гидроксильных ионов во втором периоде. [13]
Действие данных ингредиентов раствора многофункционально: так, введение щелочи также способствует смягчению минерализованной жидкости затворения, повышению кратности н стабильности пены и дисперсности пузырьков; жидкое стекло при взаимодействии с силикатными составляющими раствора и камня полимеризустся с образованием поликремниевой кислоты, что приводит к снижению проницаемости раствора и камня, а также повышению тампонирующей способности раствора и водотермостой-кости камня. [14]
Как показали П. С. Цыганков и Ю. Д. Слива [5], улучшение показателей спирта при введении щелочи в спирт только кажущееся. Щелочь придает спирту неприятную горечь. [15]
Страницы: 1 2 3 4