Прочность - кристаллическая решетка
Cтраница 4
С атомным строением металлов тесно связаны их прочностные свойства. Теоретически мерой прочности кристаллической решетки при разрушении является величина междуатомной связи. [46]
Электроны и положительные ионы металла взаимно связывают Друг друга; электроны не могут покинуть пределы металла благодаря притяжению к положительно заряженным атомам металла, а кржэрадляческая решетка оставленная из этих атомов, не разлетается благодаря цементирующему действию электронного газа. Так как силы, обеспечивающие устойчивость и прочность кристаллических решеток металлов, имеют несколько иной, специфический характер, то эти решетки вцделяют в особую группу. [47]
Между отдельными атомами кристаллической решетки существуют электронные связи, образованные внешними ( валентными) электронами, которые становятся как бы общими для двух соседних атомов. Орбиты этих электронов охватывают ядра соседних атомов, обеспечивая прочность кристаллической решетки. [48]
Для веществ с ионной связью характерна ионная кристаллическая решетка, в узлах которой находятся разноименно заряженные ионы, геометрически правильно расположенные относительно друг друга и связанные силами электростатического притяжения. В результате этого кулоновские силы, действующие между ионами, обеспечивают прочность кристаллической решетки и на отрыв ионов требуется довольно большая затрата энергии. В зависимости от размера и заряда иона вокруг него может группироваться разное число ионов другого знака. Это число носит название координационного числа. [49]
Значения ионизационных потенциалов ( и энергий присоединения электронов) важны не только для ряда расчетов, в том числе для расчета энергии решетки по уравнению Борна. Из этих данных наглядно следует одна из причин ограниченной применимости ионной модели в расчетах прочности кристаллической решетки. [50]
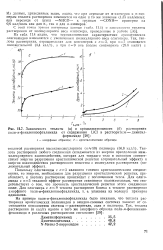 |
Зависимость теплоты ( а и продолжительности ( б растворения поли-лг-фениленизофталамида от содержания LiCl в растворителе - диметил. [51] |
Поскольку олигоамиды с п3 являются типично кристаллическими соединениями, то энергия, необходимая для разрушения кристаллической решетки, преобладает, и поэтому растворение происходит с поглощением тепла. Для олиго-амида с я5 тепловой эффект растворения становится положительным, что свидетельствует о том, что прочность кристаллической решетки этого соединения ниже. [52]
Могут сказаться соответствующее валентное состояние элемента, какие-то причины, связанные с электронами, или же прочность кристаллической решетки. [53]
Скорость стеклообразования зависит от свойств растворяющегося вещества - кварцевых зерен и свойств растворителя - силикатного расплава. Она увеличивается с уменьшением величины зерен кварца, с отклонением формы зерен от шаровых, а также при наличии включений, нарушающих прочность кристаллической решетки кварца. Продолжительность стеклообразования сокращается с уменьшением вязкости расплава и его поверхностного натяжения, которые в свою очередь изменяются от состава стекол. [54]
Таким образом, возникновение ойъемно-центрированных кубических структур или высокотемпературных модификаций у простых металлов I и II групп и у переходных металлов IV, V и VI периодов, ланта-нидов и актинидов имеет общую причину - - конфигурацию внешних электронов их металлических ионов. В рядах К-Cr, Rb-Mo, Cs - W сильно возрастают температуры плавления, модуль упругости и твердость, характеризующие рост сил межатомной связи Повышение прочности кристаллической решетки внутри групп от Ti, V, Cr соответственно к Hf, Та, W объясняется повышением концентрации электрояисто газа вследствие уменьшения размеров металлических ионов. [55]
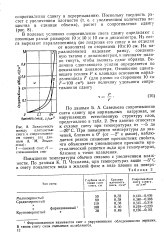 |
Зависимость между плотностью снега и сопротивлением сдвигу ( по данным А. М. Эльме-ссва. [56] |
Эти данные относятся к сухому снегу при температурах от - 5 до - 120 С. При повышении температуры до значений, близких к 0 ( от - 2 и выше), наблюдается резкое снижение прочностных свойств, что объясняется уменьшением прочности кристаллической решетки льда при температурах, близких к точке плавления. Повышение температуры обычно связано с увеличением влажности. [57]
Страницы: 1 2 3 4