Прочность - связь - вода
Cтраница 1
 |
Зависимость свободной энергии от степени дисперсности. [1] |
Прочность связи воды с частицами у обоих видов гидратации, очевидно, неодинакова. Целесообразно, как в случае ионных, так и граничных сольват-ных слоев, различать первичную ( более прочно связанную) и вторичную гидратации. [2]
Прочность связи воды гигроскопической и воды кристаллогидратов различна, поэтому скорость взаимодействия с карбидом кальция этих двух форм воды в породе неодинакова. При комнатной температуре гигроскопическая вода успевает прореагировать с карбидом кальция в течение 15 - 30 сек, тогда как-кристаллизационная вода солей за это время в реакцию практически не вступает. Это различие дает возможность производить раздельное определение содержания в породе этих двух форм воды. [3]
 |
Зависимость свободной энергии от степени дисперсности. [4] |
Прочность связи воды с частицами у обоих видов гидратации, очевидно, неодинакова. Целесообразно, как в случае ионных, так и граничных сольват-ных слоев, различать первичную ( более прочно связанную) и вторичную гидратации. [5]
В зависимости от прочности связи воды в кристаллогидратах их плавление может протекать конгруэнтно или инконгруэнтно. В первом случае не наблюдается дегидратация ионов соли вплоть до достижения температуры плавления и расплав находится в равновесии с исходным кристаллогидратом. Соединения, которые плавятся инконгруэнтно, полностью или частично дегидратируются ниже температуры плавления; в этом случае расплав находится в равновесии с двумя кристаллогидратами различного состава или с кристаллогидратом и безводной солью. [6]
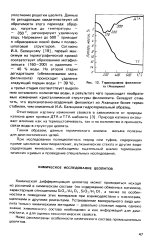
Исследования показали, что прочность связи воды в гидратах колеблется в широких пределах. Потеря воды гидратами, стабильными при наиболее высоких давлениях водяного пара, по сравнению с потерей воды гидратами, устойчивыми при более низких давлениях, показана кривыми изо-термического разложения на фиг. [7]
Молекулярная теплота гидратации - мера прочности связи воды в цеолитах. В натролите переход от насыщенного состояния с i.6 молекулами воды к продукту с 14 молекулами воды сопровождается быстрым возрастанием теплоты гидратации, которая затем остается постоянной со значением 25 жал / моль до полной дегидратации. В случае томсонита тепловой эффект отчетливо различен в интервале числа молекул воды от 12 до 8 и от 8 до 4; в случае гидрата с четырьмя молекулами воды теплота гидратации составляет около 30 ккал / моль. Следовательно, плавная кривая натролита указывает на одинаковость связи всех молекул воды, тогда как в томсоните можно выделить различные группы через каждые четыре молекулы воды. [8]
В настоящей статье изложены результаты исследования прочности связи воды и катионов с активными центрами и адсорбции анионов из растворов солей и кислот. Последнее, по-видимому, позволило бы ближе подойти к раскрытию роли гидроксильной группы воды, участвующей в обмене с анионом. [9]
 |
Термограмма филлипси-та ( Ахалцихе. [10] |
Природа катиона оказывает влияние как на термоустойчивость, так и на количество и прочность связи воды в структуре цеолита. [11]
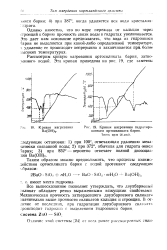 |
Кривая нагревания гидратнро-ванного ортосиликата бария. [12] |
Однако известно, что по мере перехода от кальция через стронций к барию прочность связи воды в гидратах увеличивается. Это дает нам основание предполагать, что вода из гидроокиси бария не выделяется при какой-либо определенной температуре, л удаление ее происходит непрерывно и заканчивается при более высоких температурах. [13]
В основу разработанных во ВНИИГе методов химического фазового анализа соляных пород положены такие свойства минералов, как скорость растворения их в водно-солевых растворах и прочность связи воды в различных кристаллогидратах. [14]
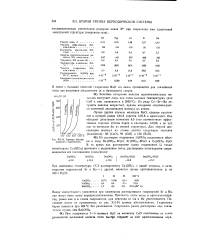 |
Кривые обезво - г., ., 0 / / - чп ои г / - / - чг tr / -. [15] |
Страницы: 1 2