Прочность - связь - водород
Cтраница 2
Ингибитор в таком случае быстро расходуется и уже не препятствует цепной реакции окисления. В силу этого существует определенный оптимум прочности связи водорода в ингибиторе. [16]
Поляризующее же влияние заместителей на прочность связи металла с кислотным остатком в его солях выяснено еще в недостаточной мере. Оно не всегда имеет одинаковый характер в сравнении с изменением прочности связи водорода, замещающегося металлом. Установление этой зависимости в случае введения в молекулу электроноакцептор-ных заместителей затрудняется элиминированием поляризующего влияния эффектом утяжеления. [17]
Изложенное иллюстрируем также наглядной, но условной схемой, имеющей чисто качественный характер. В левой половине схемы обозначены вещества в такой последовательности, что прочность связи водорода в их молекулах растет сверху вниз. В той же последовательности растет сродство к протону молекул растворителей, поименованных в правой половине схемы. [18]
 |
Диаграмма состояния системы Zr-H. [19] |
За последнее время показана способность гидрида титана при легировании другими переходными металлами - V, Nb и Мо - давать широкие области тройных твердых растворов. Изучение нейтронографическим методом [290], методом неупругого рассеяния нейтронов [293] и методом ПМР [294] показывает также изменение перераспределения водорода по тетраэдриче-ским и октаэдрическим пустотам решетки и параллельное уменьшение прочности связи водорода. Эти данные можно интерпретировать как изменение валентного состояния водорода. Спектр протонного магнитного резонанса показал две линии - широкую, отвечающую тетраэдрически расположенному водороду, и узкую, отвечающую водороду в октаэдрических пустотах; интенсивность последней линии возрастает по мере увеличения содержания второго металла - ванадия, ниобия или молибдена. [20]
Ввиду того что растворитель также участвует в ионизации в качестве кислоты или основания, ионизация определяется протолитиче-скими особенностями не только растворенного вещества, но и растворителя. В разных растворителях ионизация кислоты или основания может сильно изменяться; мало того, вещество, ионизированное в одном растворителе как кислота, в другом окажется ионизированным как основание ( или обратно) в зависимости от сродства молекул растворенного вещества и растворителя к протону и от прочности связи водорода в их молекулах. [21]
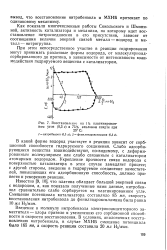 |
Восстановление на 1 % платинированном угле ( 0 3 г в 75 % этиловом спирте при. [22] |
В какой форме водород участвует в реакции зависит от сорб-ционной способности гидрируемого соединения. Слабо адсорбирующиеся вещества взаимодействуют, по-видимому, с деформированным молекулярным или слабо связанным с катализатором атомарным водородом. Укрепление прочности связи водорода с поверхностью катализатора в этом случае замедляет процесс; с другой стороны, введение в гидрируемое соединение заместителей, повышающих его адсорбционную способность, должно привести к ускорению реакции. [23]
 |
Зависимость количества водорода, выделяющегося из электролитического никеля, от температуры. [24] |
Пр-и повышении температуры нагрева обычных образцов с 300 до 900 С количество экстрагируемого газа увеличивается почти в четыре раза, в то время как для облученных образцов это изменение незначительно. Таким образом, для полного удаления газа из об - - лученного образца достаточно-нагревать его при температурах 300 или 500 С в течение-30 мин. Все это говорит о том, что прочность связи водорода с металлом, осажденным в ультразвуковом поле, слабее, чем с осадком, полученным в обычных условиях. [25]
Если радикалы R - реагируют преимущественно но первой схеме, то молекулы МП есть передатчики цепи. Если же эта реакция протекает с малой скоростью, то Г1Н есть ингибиторы. Поскольку это зависит от относительной реакционной способности радикалов и прочности связи водорода, может оказаться, что одно и то же соединение будет то передатчиком цени, то ингибитором. [26]
По тепло-там адсорбции металлы могут быть расположены в следующий ряд Ir Fe Pt Ni Rh Ru Co. Однако совершенно очевидно, что медь адсорбирует водород с образованием связи, прочность которой сравнима с прочностью связи водорода с другими переходными металлами. Адсорбция на никеле представляет собою, очевидно, относительно простой случай; для других металлов общая картина осложнена иными типами адсорбции. Некоторые из этих металлов будут рассмотрены ниже более подробно. [27]
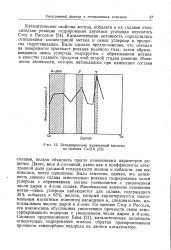 |
Дегидрирование муравьиной кислоты на сплавах Cu / Zn.. [28] |
Далее, веса d - состояний, равно как и коэффициенты электронной доли удельной теплоемкости железа и кобальта, как выяснилось, почти одинаковы. Было замечено, однако, что активность данного сплава относительно реакции гидрирования окиси углерода с образованием метана уменьшается с увеличением числа дырок в с. Минимальное значение отношения метан-окись углерода наблюдается для сплава, содержащего 35 % кобальта и 65 % железа, который характеризуется максимальным магнитным моментом насыщения и, следовательно, максимальным числом дырок в rf - зоне. По мнению Стоу и Рассела, эта взаимосвязь обусловлена увеличением прочности связи хемо-сорбированного водорода с увеличением числа дырок в с. Согласно предположению Бика [31], каталитическая активность относительно гидрирования этилена обратно пропорциональна прочности хемосорбции водорода на данном катализаторе. [29]
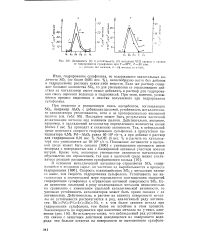 |
Активность ( У и устопчиьость ( 2 металлов VIII группы в процессе гидрирования сульфолена при Г 20 С, Р 50 атм. а - металлы без носителя. 6 - 2 % металла на у - АЬОз. [30] |
Страницы: 1 2 3