Дигидрофуран
Cтраница 1
Дигидрофуран и СН3СН ( ОС2Н5) 2 дают 2-этокси - 3 - ( 2-этоксипропил) - тетрагидрофуран. Дигидропиран с СН3СН ( ОСН3) 2 и BF3 - 0 ( C2H6) 2 образует 2-метокси - 3 - ( 2-метоксипро-пил) - тетрагидропиран. [1]
Дигидрофуран и СН3СН ( ОС2Н5) 2 дают 2-этокси - 3 - ( 2-этоксипропил) - тет-рагидрофуран. Дигидропиран с СН3СН ( ОСН3) 2 и BF3 - O ( C2H5) 2 образует 2-метокси - 3 - ( 2-метоксипропил) - тетрагидропиран. [2]
Дигидрофуран реагирует с акролеином, давая соединение СтНюОз, реакция этого соединения с води. [3]
Сам А3 - дигидрофуран неспособен к необратимому катализу Н. Д. Зелинского в обычных его условиях. [4]
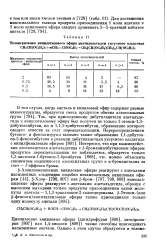 |
Телоиеризация винилэтилового эфира диэтилацеталем уксусного альдегида. [5] |
Циклические виниловые эфиры ( дигидрофуран [800], дигидропи-ран [807] или 1 4-диоксен [809]) также способны присоединять насыщенные ацетали. [6]
При дегидратировании бутендиола-1 4 образуется дигидрофуран; при гидрати ровании его получают эритрит. При взаимодействии с синильной кислотой и последующем гидрировании бутен-диол-1 4 превращается в гексаметилендиамин. [7]
Неполный гидрид фурана - Д3 - дигидрофуран при действии аммиака дает смесь пиррола и пирролидина, при действии сероводорода - смесь тиофена и тиофана [1, 2], возникающих в результате необратимого катализа Д3 - дигидропирролидина и соответственно А3 - дигидротиофена, образующихся из А3 - дигидрофурана. Сам А3 - дигидрофуран неспособен к необратимому катализу Н. Д. Зелинского в обычных его условиях. [8]
Винберг [304] получил ( 3-фенилфуран при дегидрировании замещенного дигидрофурана LXVII серой в кипящем диметилформ-амиде. Артемазулен LXVIII [56,103,189] и линдеразулен LXIX [28, 56, 103] образуются при дегидрировании и, в некоторых случаях, прициклизации соответствующихпроизводных гваианолидов. [9]
Однако циклические виниловые эфиры, например дигидропиран или дигидрофуран, отличаются в этом отношении от винилалки-ловых эфиров. Дигидропиран и дигидрофуран конденсируются с ацеталями алифатических насыщенных альдегидов в обычных условиях, но даже при эквимолярных соотношениях компонентов вторичные продукты либо не образуются вовсе, либо получаются в небольших количествах. [10]
Выведение водорода из зоны реакции через катализатор ускоряет дегидрирование дигидрофурана в фуран, а при отсутствии водорода на поверхности катализатора превращений дигидрофурана при прочих постоянных условиях не происходит. [11]
Типичными мономерами этого типа являются простые виниловые эфиры, изобути-лен и дигидрофуран. С другой стороны, мономеры с электроно-акцепторными заместителями при ненасыщенном атоме углерода имеют тенденцию полимеризоваться по анионному механизму. Полимеризация олефинов, содержащих сильноактивированную двойную связь ( таких, как винилидендицианид) катализируется даже слабыми основаниями, хотя для большинства мономеров, полимеризуемых по анионному механизму, используют сильные основания. Между этими двумя предельными типами мономеров лежит большое число ос-замещенных олефинов, которые содержат в крайнем случае лишь слабоэлектроноакцеп-торные заместители и пол-имеризуются по свободнорадикальному механизму. [12]
В очень мягких кислотных условиях 309 подвергается быстрой конверсии в производное дигидрофурана 313 ( через промежуточное образование 309а), а конверсия 310 - [ ЗЮа ] - 314 происходит при действии диэтиламина в ТГФ. В обоих случаях указанный каскад реакций легко протекает при комнатной температуре. Таким образом, ключевые химические события, происходящие при взаимодействии антибиотика 293 с ДНК, а именно внутримолекулярное присоединение по Михаэлю с последующей спонтанной циклизацией ендиина п бирадикальный интер-мсдиат, удалось воспроизвести на специально сконструированной модели. [13]
В очень мягких кислотных условиях 309 подвергается быстрой конверсии в производное дигидрофурана 313 ( через промежуточное образование 309а), а конверсия 310 - [ ЗЮа ] - 314 происходит при действии диэтиламина в ТГФ. В обоих случаях указанный каскад реакций легко протекает при комнатной температуре. Таким образом, ключевые химические события, происходящие при взаимодействии антибиотика 293 с ДНК, а именно внутримолекулярное присоединение по Михаэлю с последующей спонтанной циклизацией ендиина в бирадикальный интер-мсдиаг, удалось воспроизвести на специально сконструированной модели. [14]
В очень мягких кислотных условиях 309 подвергается быстрой конверсии в производное дигидрофурана 313 ( через промежуточное образование 309а), а конверсия 310 - [ ЗЮа ] - 314 происходит при действии диэтиламина в ТГФ. В обоих случаях указанный каскад реакций легко протекает при комнатной температуре. Таким образом, ключевые химические события, происходящие при взаимодействии антибиотика 293 с ДНК, а именно внутримолекулярное присоединение по Михаэлю с последующей спонтанной циклизацией ендиина в бирадикальный интер-медиат, удалось воспроизвести на специально сконструированной модели. [15]
Страницы: 1 2