Радиус - анион
Cтраница 2
Мюррею [323], окислы с высоким отношением радиусов анионов и катионов, например MgO, имеют более значительную величину угла смачивания О данным металлом, чем окиси, у которых отношение Ra. Для окисей с большими катионами сделано предположение, что катионы активны на промежуточных поверхностях и таким образом способствуют уменьшению угла смачивания. [16]
Образование аниона BF4 - сопровождается некоторым уменьшением радиуса аниона по сравнению с В03 - - и падением его заряда с 3 - до 1 -, что приводит к резкому уменьшению плотности заряда на поверхности аниона. В то же время радиус BF4 - значительно больше радиуса F - в анионе плавиковой кислоты. [17]
Обратная перестройка наблюдается при увеличении давления, когда радиус аниона уменьшается быстрее, чем радиус катиона, - происходит сближение размеров ионных радиусов, которое может привести к переходу кристалла из примитивной кубической решетки в объемноцентрированную. Такого рода перестройка кристаллической структуры при повышении давления наблюдается у хлористого, бромистого и йодистого калия, бромистого и йодистого рубидия. [18]
Если из рассчитанных таким путем расстояний а вычесть кристаллографический радиус анионов, получаются эффективные радиусы катионов. [19]
Как меняется сила бескислородных кислот в зависимости от радиуса аниона. [20]
В этом ряду возрастание силы кислот обусловлено возрастанием радиуса аниона при неизменном его заряде. [21]
Четкость картин дифракции на щелочно-галоидных кристаллах объясняется различием радиусов анионов и катионов в них. [23]
Из приведенных представлений следует, что с увеличением радиуса аниона энергия гидратации убывает сильнее, чем энергия кулоновского взаимодействия, что приводит к росту адсорбции и флотационной способности собирателя. Поэтому иодид натрия в отличие от хлорида флотируется. С другой стороны, увеличение заряда катиона уменьшает адсорбцию и флотационную способность собирателя. По этой причине галогениды щелочноземельных металлов не флотируются, несмотря на то, что у ионов Ва2 и аминной головки радиусы даже одинаковы. [24]
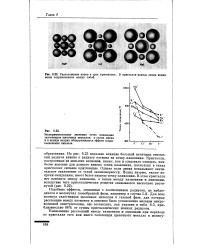 |
Расположение ионов в трех кристаллах. В кристалле иодида лития иодид-ионы соприкасаются между собой. [25] |
На рис. 6.23 показано влияние большой величины отношения радиуса аниона к радиусу катиона на точку плавления. Кристаллы, построенные из меньших катионов, имеют, как и следовало ожидать, наиболее высокие для данного аниона точки плавления, поскольку в таких кристаллах сильнее притяжение. Однако соли лития показывают значительное отклонение от такой закономерности. Иодид натрия, также вопреки ожиданиям, имеет более низкую точку плавления. [26]
Для каждого расположения приведено отношение радиуса катиона к радиусу аниона ( отношение радиусов), соответствующее плот-нейшей упаковке; это отвечает контакту между анионами, а также между анионами и катионом, причем как анионы, так и катион рассматриваются как сферы. [28]
При ух, За2Ь направление реакции зависит от значений радиусов анионов и разности значений радиусов катионов. [29]
Таким образом, координационное число определяется соотношением между размерами радиусов анионов и катионов в структуре. [30]
Страницы: 1 2 3 4

