Радиус - атом
Cтраница 3
Радиус атома: чем он больше, тем дальше от ядра находятся периферические электроны, тем менее прочно они связаны с атомом, тем сильнее выражены металлические свойства элемента. [31]
Радиусы атомов сравнительно большие. Этим объясняется их высокая химическая активность как металлов. [32]
Радиусы атомов и ионов элементов средние между щелочноземельными металлами и элементами подгруппы галлия и увеличиваются от скандия к актинию. Сила их восстановительных свойств также является средней между щелочноземельными металлами и семейством галлия и растет от скандия к актинию. [33]
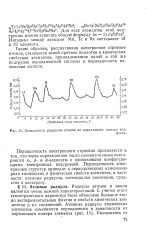 |
Зависимость радиусов атомов от порядкового номера элемента. [34] |
Радиусы атомов и ионов являются очень важной характеристикой. С учетом этого геометрического параметра было объяснено большое число экспериментальных фактов и свойств химических элементов и их соединений. [35]
 |
Схема действия спектрографа. [36] |
Радиусы атомов имеют значения порядка 100 пм. [37]
Радиусы атомов и ионов являются очень важной характеристикой. С учетом этого геометрического параметра объяснено большое число экспериментальных фактов и свойств химических элементов и их соединений. Уменьшаясь от щелочного металла до галогена, атомный радиус следующего щелочного металла снова увеличивается и становится больше радиуса атома предыдущего щелочного. Так, атом натрия имеет радиус 0 186 нм, магния - 0 16 нм, хлора - 0 099 нм, а радиус атома калия вновь увеличивается и становится равным 0 231 нм. [38]
Радиусы атома и иона гафния Ш4 меньше, чем у циркония ( табл. 32) вследствие лантаноидного сжатия. [39]
Радиусы атомов и отрицательно заряженных ионов закономерно увеличиваются от фтора к иоду в соответствии с увеличением числа энергетических уровней. [40]
Радиусы атома и ионов германия, Величины радиусов атома и ионов германия, полученные различными исследователями, расходятся. [41]
Радиусы атомов и их восстановительная способность уменьшается ( окислительная способность возрастает); свойства простых тел изменяются от металлических до металлоидных. Элементы обладают значительным сходством некоторых своих свойств. [42]
Радиусы атомов имеют значения порядка 100 пм. [43]
Радиусы атомов составляют 0 3 - 3 А. [44]
Тетраэдриче-ские радиусы атомов показаны на фиг. Германий, например, замещает в антимониде галлия сурьму, а в арсениде индия - индий. Исключениями являются Ge и Si в антимониде индия, где они, как оказалось, замещают сурьму. По-видимому, IV-атомы могут также входить в решетку парами, замещая соседние разноименные атомы и образуя таким образом нейтральные центры. Например, выяснилось, что атомы Ge ( 2 44 А) и Si ( 2 34 А) входят парами в GaAs ( 2 44 А), достигая больших концентраций, но в InAs ( 2 62 А) они замещают только атомы индия. [45]
Страницы: 1 2 3 4