Металлический радиус
Cтраница 4
Увеличение заряда ядра атома бериллия по сравнению с зарядом ядра атома лития наряду с тем, что 25-электроны только частично экранируют друг друга, приводит к двум эффектам: 1) атом Be имеет металлический радиус только 0 89 А, значительно меньше, чем в случае лития ( 1 22 А); 2) потенциалы ионизации Be, 9 32 и 18 21 эв, гораздо большие, чем у Li ( 5 39 эв), делают Be значительно менее электроположительным, если рассматривать его химические свойства в сравнении со свойствами Li. Действительно, не существует никаких кристаллических соединений или растворов, в которых ионы Ве2 существовали бы как таковые. Все соединения, строение которых было определено, даже соединения с наиболее электроотрицательными элементами, такие, как ВеО и BeF2, по крайней мере частично обладают ковалентным характером связи. Электронное строение атомов других элементов II группы ( Mg, Ca, Sr, Ba и Ra) подобно строению атома Be. Однако больший размер этих атомов уменьшает влияние заряда ядра на валентные электроны. Так, их потенциалы ионизации ниже, чем у Be; они в основном более электроположительны, а ионная природа их соединений закономерно возрастает в группе сверху вниз. [46]
Увеличение заряда ядра атома бериллия по сравнению с зарядом ядра атома лития наряду с тем, что 2з - электроны только частично экранируют друг друга, приводит к двум эффектам: 1) атом Be имеет металлический радиус только 0 89 А, значительно меньше, чем в случае лития ( 1 22 А); 2) потенциалы ионизации Be, 9 32 и 18 21 эв, гораздо большие, чем у Li ( 5 39 эв), делают Be значительно менее электроположительным, если рассматривать его химические свойства в сравнении со свойствами Li. Действительно, не существует никаких кристаллических соединений или растворов, в которых ионы Ве2 существовали бы как таковые. Все соединения, строение которых было определено, даже соединения с наиболее электроотрицательными элементами, такие, как ВеО и BeF2, по крайней мере частично обладают ковалентным характером связи. Электронное строение атомов других элементов II группы ( Mg, Ca, Sr, Ba и Ra) подобно строению атома Be. Однако больший размер этих атомов уменьшает влияние заряда ядра на валентные электроны. Так, их потенциалы ионизации ниже, чем у Be; они в основном более электроположительны, а ионная природа их соединений закономерно возрастает в группе сверху вниз. [47]
Радиус иона растет с увеличением отрицательного заряда и падает с ростом положительного заряда. Металлические радиусы в пределах одного периода уменьшаются от щелочного металла до металла VIII группы, а далее растут менее значительно. [48]
Америций и кюрий - значительно более легкие металлы, а температуры их плавления выше, чем урана, нептуния и плутония. Металлический радиус калифорния показывает, что он двухвалентен, подобно европию и иттербию. [49]
Отсюда следует, что значительная часть поверхности электрода занята атомами ртути. Металлический радиус атома Hg примерно на 0 2 А больше, чем Ga. Поэтому можно предположить, что ионы гидроксония не могут приблизиться к атомам галлия на такое же расстояние, как на поверхности чистого металла. Это затрудняет туннелирование и повышает соответственно кинетический изотопный эффект при разряде на атомах галлия. Поскольку энергия адсорбции водорода на галлии больше, разряд на галлии легче, и суммарный изотопный эффект определяется именно увеличением S для выделения водорода на атомах Ga. При высокой же концентрации ртути поверхность электрода практически покрыта ртутью, и ее характеристики ( S, т ]) близки к таковым для чистого металла. [50]
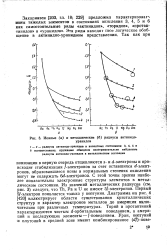 |
Ионные ( а и металлические ( б радиусы актинидо. [51] |
С этой точки зрения наиболее показательны электронные структуры элементов в металлическом состоянии. Из значений металлических радиусов ( см. рис. 3) следует, что Th, Ра и U не имеют 5 / - электронов. Первый Sf-электрон появляется только у нептуния. Диаграмма на рис. 4 [420] иллюстрирует области существования кристаллических структур и характер электронов металлов до америция включительно при различных температурах. Торий и протактиний характеризуются чистым rf - орбитальным поведением, а америций и последующие элементы - / - поведением. [52]
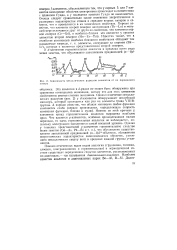 |
Зависимость металлических радиусов элементов от их порядкового номера. [53] |
Эта аналогия в d - рядах не может быть обнаружена при сравнении потенциалов ионизации, потому что для этих элементов свойственны разные степени окисления. Однако изменение металлических радиусов ( рис. 2) у с ( - элементов обнаруживает неглубокий минимум, который приходится как раз на элементы триад VIIIB-группы. Именно по этой причине у элементов триад горизонтальная аналогия выражена наиболее ярко. Что касается р-элементов, особенно принадлежащих малым периодам, то здесь горизонтальная аналогия не наблюдается, поскольку электронами заполняется самый внешний уровень. [54]
Ковалентный радиус резко возрастает при переходе от углерода к кремнию, а затем при движении к олову обнаруживается зигзагообразный характер кривой. Те же зигзагообразные отклонения обнаруживают металлические радиусы. Ветвь кривой для d - переходных металлов титан, цирконий, гафний) располагается левее ветви для элементов главной подгруппы, причем цирконий и гафний имеют близкие атомные радиусы, а титан значительно меньший, вследствие чего точка для титана сильно отклонена вправо. Ветвь / - переходных металлов ( церий, тербий, торий) расположена слева от кривой для титана, циркония и гафния и обнаруживает характерный излом. [55]
Нужно отметить, что кривые изменения атомных радиусов не только подтверждают правомерность сдвига легких элементов первых двух периодов в таблице Менделеева, но и отражают также некоторое смещение ряда натрий-аргон влево по отношению к своим более легким аналогам, вследствие чего эти элементы представляют начало ответвления в каждой группе d - переходных металлов. Эти смещения особенно велики для металлических радиусов натрия, магния и алюминия. Вполне определенно выявляются сдвиги вправо по отношению к более тяжелым аналогам всего ряда металлов 4-го периода, от калия до цинка, причем этот сдвиг распространяется и дальше на элементы главных подгрупп 4-го периода от галлия к криптону. Совершенно определенно все редкоземельные металлы иттриевого ряда сдвинуты вправо по отношению к металлам цериевого ряда. [56]
Между такими парами ионов, как О2 - и F или S2 - и С1 -, нет большой разницы в радиусах, так как возросшее притяжение между ионами с высоким зарядом маскирует увеличение размера, которое мы могли бы ожидать с увеличением отрицательного заряда. Такое изменение обнаруживается и в металлических радиусах этих элементов ( стр. [57]
Но картина значительно меняется, если сопоставлять металлические радиусы. На участке Се-Sm сжатие равно 0 05 А. В ряду легких актиноидов от тория до плутония оно значительно больше - 0 28 А и по величине напоминает уменьшение радиусов в серии Sd-элементов. [58]
Металлические радиусы отвечают КЧ12; ковалентные радиусы КЧ-4 и одинарной связи. Для Sb и Sn кроме ковалентных приведены также и металлические радиусы. Для других значений КЧ необходимо вводить поправку: - 6 % для КЧ4; 3 % для КЧ8; 12 % для КЧ. [59]
Страницы: 1 2 3 4