Разбавление - буферный раствор
Cтраница 1
Разбавление буферного раствора водой или концентрирование его путем выпаривания также почти не изменит рН, так как не изменится соотношение концентраций компонентов, от которого зависит концентрация Н - и ОН - - ионов. Если, например, при разбавлении того же ацетатного буферного раствора водой концентрация Н - ионов уменьшается, то это уменьшение компенсируется увеличением степени диссоциации уксусной кислоты. [1]
Разбавление буферного раствора водой или концентрирование его путем выпаривания также почти не изменит величины рН, так как не изменится соотношение концентраций компонентов, от которого зависит концентрация Н - и ОН - ионов. Если, например, при разбавлении того же ацетатного буферного раствора водой концентрация Н - ионов уменьшается, то это уменьшение компенсируется увеличением степени диссоциации уксусной кислоты. [2]
 |
Буферные растворы. [3] |
При разбавлении буферного раствора водой отношение аналитических концентраций слабой кислоты и ее соли остается постоянным. Коэффициенты активности могут изменяться по-разному. Однако при разбавлении буферных растворов их рН изменяется незначительно и в ряде случаев этим изменением можно пренебречь. Этот пример показывает также, что буферные смеси можно приготовлять не только из кислоты ( или основания) и соли, но и из двух солей на разных ступенях диссоциации. [4]
При разбавлении буферного раствора водой рН изменяется очень незначительно, так как, хотя концентрация слабой кислоты или слабого основания уменьшается, концентрация образуемых ими ионов водорода или гидроксид-ионов увеличивается за счет повышения степени диссоциации электролита. Эти два процесса взаимно компенсируются, и в конечном результате концентрация ионов водорода или гидроксид-ионов сохраняется постоянной. [5]
 |
Буферные растворы. [6] |
При разбавлении буферного раствора водой отношение аналитических концентраций слабой кислоты и ее соли остается постоянным. Коэффициенты же активности могут изменяться по-разному. Однако при разбавлении буферных растворов их рН изменяется незначительно, и в ряде случаев этим изменением можно пренебречь. Этот пример показывает также, что буферные смеси можно приготовлять не только из кислоты ( или основания) и соли, но и из двух солей на разных ступенях диссоциации. [7]
При разбавлении буферных растворов также не происходит изменения рН среды, так как не происходит изменения соотношения компонентов, от которых зависит концентрация Н и ОН - буферных систем. [8]
При разбавлении буферных растворов, а также при добавлении к ним нейтральных солей незначительные изменения а обусловлены изменением величины коэффициентов активности. [9]
При разбавлении водой буферных растворов концентрация водородных ионов в них почти не изменяется. [10]
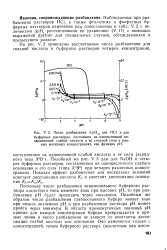 |
Число разбавления Л рН д для HCI и для буферных растворов, состоящих из одноосновной незаряженной слабой кислоты и ее сильной соли в равных молярных концентрациях, как функция рН. [11] |
Поскольку число разбавления эквимоляльного буферного раствора кислотного типа изменяет знак при высоких рН, то при разбавлении рН будет проходить через максимум. Подобным же образом число разбавления слабоосновного буфера меняет знак при низких значениях рН и при разбавлении раствора рН может пройти через минимум. В области промежуточных значений рН кривые для каждой концентрации буфера превращаются в прямые линии и число разбавления не зависит от константы диссоциации слабой кислоты или основания. [12]
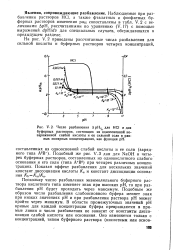 |
Число разбавления Д рНуг для НС1 и для буферных растворов, состоящих из одноосновной незаряженной слабой кислоты и ее сильной соли в равных молярных концентрациях, как функция рН. [13] |
Поскольку число разбавления эквимоляльного буферного раствора кислотного типа изменяет знак при высоких рН, то при разбавлении рН будет проходить через максимум. Подобным же образом число разбавления слабоосновного буфера меняет знак при низких значениях рН и при разбавлении раствора рН может пройти через минимум. В области промежуточных значений рН кривые для каждой концентрации буфера превращаются в прямые линии и число разбавления не зависит от константы диссоциации слабой кислоты или основания. [14]
Анализ уравнений (4.26) и (4.31) показывает, что разбавление буферных растворов практически не меняет концентрации водородных ионов ( рН) раство ра, так как отношения концентрации соли и кислоты или соли и основания, входящие в эти уравнения, при разбавлении не меняются. Очевидно, что при разбавлении растворов только кислоты или основания происходило бы пропорциональное изменение концентрации водородных ионов, если не учитывать изменения степени диссоциации. [15]
Страницы: 1 2 3