Величина - основность
Cтраница 2
До самого последнего времени основности насыщенных алифатических кетонов в основном были неизвестны. Низкие величины основности алифатических кетонов сравнимы с величинами основности ароматических кетонов, что согласуется с тем фактом, что для карбонилсодержащих оснований, таких, как карбоновые кислоты и амиды, разница в основностях алифатических и ароматических членов рядов мала. [16]
Если не принимать во внимание вопросы, затронутые в разделе IV, А, то относительные величины, приведенные в табл. 15 для одного и того же соединения, должны характеризовать силу акцептора. Считают, что влияние акцептора не является постоянным фактором, поскольку в этом случае величины основности, полученные разными методами для одного и того же метильного производного бензола, были бы приблизительно постоянными. [17]
Углубленное изучение кислотно-основных равновесий в неводных растворителях должно привести к лучшему пониманию роли растворителя в изменении этих равновесий. Вообще в тех случаях, когда речь идет о количественном изучении проблемы, предпочтительно иметь дело с величинами основности фосфинов, определенными в нитрометане. Тем не менее, исследование основности в водных средах или в средах, подобных водным, представляется важным по ряду других причин. [18]
Этот метод не получил широкого практического применения, хотя его критический анализ, проведенный Фосеттом и Криговским [41], показал, что метод правильно отражает величину основности. [19]
В качестве предельного случая укажем на ароматический амин, у которого угол sp равен или почти равен нулю, вопреки имеющемуся стерическому напряжению. Здесь спектр не покажет ингибиро-вания мезомерии, но если в ионе возможна и действительно происходит перестройка, то стерическое напряжение в молекуле будет обнаружено по величине основности. Вероятно, относительно высокая величина основности М М - диэтиланилина должна быть объяснена именно таким образом ( стр. [20]
Различие в основности К М 4-триметиланилина и хинуклидина на 5 порядков в значительной степени обусловлено делокализацией электронной пары азота по ароматическому кольцу. Это подтверждается величиной основности бензохинуклиди-на, которая больше соответствующей величины для анилина, поскольку конфигурация молекулы мешает копланарности азота с ароматическим кольцом, уменьшая тем самым делокализацию электронов. Однако это различие составляет всего лишь 102; это указывает, что разница в величинах основности анилина и хинуклидина в 103 раз может быть обусловлена индуктивным эффектом ненасыщенного кольца ( см. разд. Можно ожидать, что n - нитрозаместитель в ароматическом кольце бензохинуклидина будет оказывать меньшее влияние на основность, чем соответствующий заместитель в анилине, так как резонансные структуры типа VI ( разд. [21]
Фенильная группа, электроноакцепторная способность которой невелика, вызывает очень незначительное уменьшение р / Скисл. Введение кислотных остатков ( СООН, SO3H) в ядро акридина обусловливает образование внутренних солей ( амфотерных ионов), в результате чего свойства катиона почти исчезают даже у таких сильных оснований, как 5-аминоакри-дин. Несмотря на это, величина основности амфотерных ионов изменяется мало, а сила кислотных групп обычно несколько больше, чем в соответствующих соединениях ряда бензола. По способности образовывать амфотерные ионы при введении СООН-группы акридины напоминают пиридины и хинолины и отличаются от ароматических аминов; последние, однако, образуют амфотерные ионы, при введении 5О3Н - группы. [22]
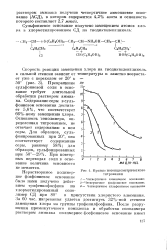 |
Кривые потенциометрического. [23] |
Превращение РН сульфониевой соли в осно-вание требует длительной обработки раствором аммиака. Содержание серы в суль-фониевом основании достигает 5 6 %, что соответствует 66 % - ному замещению хлора. Основность сополимера, определенная титрованием, не отвечает содержанию в нем серы. При повторных переводах соли в основание величина основности не меняется. [24]
Соединения акридина хорошо кристаллизуются, и большинство из них имеет отчетливо выраженные температуры плавления. Методы их синтеза не оченч сложны, однако требуют дальнейшего усовершенствования. Указанные свойства акридиновых соединений привлекают к ним внимание химиков-органиков. Физико-химиков интересуют простейшие правила, устанавливающие связь между строением и величиной основности в ряду акридинов, а также связь между строениями и спектрами поглощения. Зависимость антибактериального действия акридиновых соединений от степени ионизации представляет собой наиболее известный пример связи между физико-химическими свойствами и физиологическим действием. [25]
Средние значения молекулярного веса, получаемые такими обобщенными методами, какими являются нахождение температуры плавления, температуры кипения и осмотического давления, легко изменяются при определении в присутствии даже небольших количеств низкомолекулярных веществ. Ввиду трудности подбора удовлетворительных-растворителей имеется мало надежных данных по определению молекулярного веса гуминовых кислот, полученных из любого источника. Оден [33] определил эквивалентный вес гуминовых кислот, выделенных из торфа, при помощи электрометрического титрования и вычислил молекулярный вес по величине основности. [26]
Очевидно, что законность только тогда приобретет некоторую общность, доказательность, когда она будет выражена не только относительно мало измеримых или еще не поддающихся измерению свойств, а когда она относится к свойствам предмета, уже подвергшимся измерению. Например, свойство кислотности или основности, свойство одного элемента давать кислоты, а другого - основание до сих пор не поддается точному выражению. Мы ясно совершенно видим, что хлор есть представитель кислотных элементов, натрий, калий и их аналоги суть представители щелочных. Какие единицы к этому применять и какой тут аршин приложить к делу для того, чтобы измерить величину кислотности или величину основности элемента. Не таковы атомные веса; мы видели, что история химии привела после закона Аво-гадро - Жерара к совершенно точным, несомненным, безусловным атомным весам, не таким, которые выражали бы абсолютные атомные веса, а таким, которые выражают относительные величины тех наименьших количеств элементов, которые вступают в соединение. [27]
На деле оказывается, что противоречие лежит лишь в определениях. Мы уже указывали, что основность растворителя, по уравнению 13, включает в себя эффект диэлектрической постоянной наряду с эффектом, который, за неимением лучшего названия, мы можем назвать внутренней основностью растворителя. Хаммет имел в виду только последний эффект. Так, увеличение основности растворителя, с точки зрения Хестона и Холла, а также Кольтгофа, понижает протонную активность, сдвигая реакцию 25 дальше направо. Это должно приводить к увеличению Ка - Однако, согласно табл. 4, переход к более основному растворителю с более высокой диэлектрической постоянной должен сместить реакцию 25 налево. Так, если измерять основность растворителя, определяемую по уравнению 13, с помощью раствора кислоты, не имеющей заряда, а затем этой же величиной основности воспользоваться в том же уравнении, когда изучаемая кислота относится к типу кислот с положительным заря дом, то предсказанная таким путем величина кислотности раствора окажется совершенно ошибочной. [28]
Страницы: 1 2