Величина - концентрационная поляризация
Cтраница 2
Из уравнения ( 38) следует, что и в случае анодного растворения металла величина концентрационной поляризации находится в логарифмической зависимости от плотности тока, Предлогарифмический коэффициент зависит при этом от числа электронов, освобождающихся при ионизации одного ион-атома металла, и температуры. [16]
Из уравнения ( 38) следует, что и в случае анодного растворения металла величина концентрационной поляризации находится в логарифмической зависимости от плотности тока. Предлогарифмический коэффициент зависит при этом от числа электронов, освобождающихся при ионизации одного ион-атома металла, и температуры. [17]
Вполне естественно поэтому, что для небольших содержаний ионов висмута ( 0 125 - 0 25 TV) величина концентрационной поляризации должна быть весьма значительной. [18]
Следует отметить, что в случае поликристаллических осадков, когда образующиеся вокруг растущих кристаллов диффузионные слои перекрывают друг друга, величина концентрационной поляризации изменяется с величиной поляризующего тока. [19]
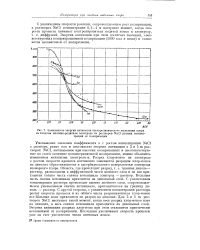 |
Зависимость энергии активации электролитического выделения хлора на гладком платино-родиевом электроде из растворов NaCl разных концентраций от поляризации. [20] |
Уменьшение значения коэффициента а с ростом концентрации NaCl в растворе, равно как и постоянство энергии активации в 3 и 5 m растворах NaCl, наблюдаемое при высоких поляризациях и несоответствующее по своей величине концентрационной поляризации, можно объяснить изменением механизма электролиза. Разряд хлор-ионов на электроде с ростом скорости процесса постепенно заменяется разрядом хлор-ионов на диполях образовавшегося и адсорбированного поверхностью электрода атомарного хлора. Большая часть скачка потенциала приходится на диполышй слой. С увеличением концентрации раствора происходит сжатие двойного слоя, сопровождающееся уменьшением скачка потенциала, приходящегося на границу диполь - раствор. С другой стороны, с увеличением концентрации раствора растет скорость процесса и из общего числа разряжающихся хлор-ионов все большая доля приходится на разряд на диполях. Для 3 и 5 m растворов NaCl наступает такой момент, когда весь разряд хлор-ионов идет на диполях, а весь скачок потенциала приходится на дипольный слой. Энергия активации разряда хлор-иона при этом становится практически независимой от поляризации. Последпяя увеличивает скорость процесса уже за счет увеличения числа активных ионов. [21]
В технических электролизах в одних случаях приходится принимать меры для уменьшения химической и концентрационной поляризации, например при электролитическом получении водорода ( так как высокая поляризация при электролизе вызывает дополнительный расход электрической энергии на протекание процесса), в других, наоборот, стремятся увеличить поляризацию, например при электроосаждении металлов в гальванотехнике, так как это позволяет получить более высокого качества осадки металлов. Величина концентрационной поляризации может быть уменьшена перемешиванием раствора. Вредное действие химической поляризации устраняется добавлением окислителей или восстановителей, которые называются деполяризаторами. Деполяризаторы широко применяются для проведения различных электрохимических реакций органического синтеза, а также в различных гальванических элементах. [22]
Существенным является также вопрос о том, насколько возможно компенсировать снижение скорости процесса, которое происходит вследствие растворения осадка в анодные промежутки времени, увеличением рабочей плотности тока. Из сравнения величин концентрационной поляризации при электролизе постоянным и реверсивным токами в случае равных средних скоростей процессов ( рис. 3, 4, 5) следует, что при малой частоте переключения тока процесс не только не интенсифицируется, но несколько замедляется. При больших частотах переключения скорость электролиза реверсивным током близка к скорости электролиза постоянным током. [23]
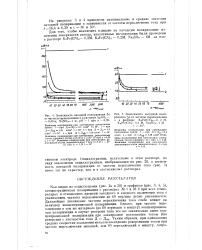 |
Зависимость катодной поляризации Де от частоты переключения п в растворе AgNOa - - 0 05м, NaN03 - 1 м, рН 1 при к 6 39.| Зависимость катодной поля. [24] |
Как видно из осциллограмм ( рис. 2а и 26) и графиков ( рис. 3, 4, 5), концентрационная поляризация г. растворах № 1 и № 2 при всех температурах и отношениях времени катодного и анодного включения тока с увеличением частоты переключения до 60 пер / мин резко уменьшается. Дальнейшее увеличение частоты переключения тока слабо влияет на величину концентрационной поляризации. [25]
Исследования поляризации и перенапряжения на отдельных электродах имеют большое теоретическое и практическое значение. В технических электролизах в одних случаях приходится принимать меры для уменьшения химической и концентрационной поляризации, например, при электролитическом получении водорода ( так как высокая поляризация на электролизе вызывает дополнительный расход электрической энергии на протекание процесса), в других, наоборот, стремятся увеличить поляризацию, например, при электроосаждении металлов в гальванотехнике, так как это позволяет получить более высокого качества осадки металлов. Величина концентрационной поляризации может быть уменьшена перемешиванием раствора. Вредное действие химической поляризации устраняется добавлением окислителей или восстановителей, которые называются деполяризаторами. Катодными деполяризаторами служат окислители, анодными - восстановители. Деполяризаторы широко применяются для проведения различных электрохимических реакций органического синтеза, а также в различных гальванических элементах. [26]
Исследования показали, что поляризация электродов является диффузионным явлением. На основе диффузионной теории и положения о двойном электрическом слое на поверхности электродов было показано, что при прохождении переменного тока через раствор происходят периодические изменения концентрации в соответствии с частотой тока. Количественно величина концентрационной поляризации зависит от изменения потенциала электрода вследствие изменения концентрации потенциалобразующих ионов у его поверхности. Из-за концентрационной поляризации ток и потенциал сдвигаются по фазе. [27]
Присутствие в электролите ПАВ усугубляет увеличение концентрационной поляризации. Объяснение этому находим в специфичности действия ПАВ, пленка которого, адсор-бировавшись на поверхности металла, сдерживает переход ионов металла в электролит, повышая их концентрацию в прианодном слое. Однако величина концентрационной поляризации в общем значении анодной поляризации занимает небольшое место. [28]
Существенное различие, однако, состоит в том, что при данном токе величина концентрационной поляризации на аноде меньше, чем на катоде. При неизменной толщине диффузионного слоя ток, плотность которого достаточна для того, чтобы в данном растворе у катода концентрация ионов М понизилась почти до нуля, проходя в том же растворе через анод из металла М, который при этом переходит в раствор в виде ионов М, вызовет лишь удвоение концентрации. Так как величина концентрационной поляризации зависит от отношения концентрации ионов вблизи поверхности к концентрации в объеме электролита, то, как показано выше, это отношение при одинаковых условиях гораздо больше на катоде, чем на аноде. К этому же выводу можно прийти другим путем, применяя ход рассуждений, который проводился при определении изменения концентрации на катоде. [29]
При очень малых значениях Дф, при которых In Д пропорционален Дф, зависимость между / 1 ф и Дф имеет приближенно линейный характер. Для значений Дф, при которых 1пДф нельзя апроксимировать линейной зависимостью, эффективная энергия активации изменяется по логарифмическому закону. При очень больших значениях Дф, при которых величина концентрационной поляризации велика, а значит, члеп, учитывающий конвективно-диффузионное поле становится сравнимым или велик по сравнению с потенциалом поляризации, АЭф очень медленно и почти совсем не изменяется с измененном потенциала поляризации. [30]
Страницы: 1 2 3