Величина - потенциал
Cтраница 2
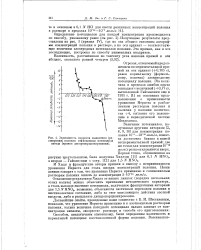 |
Зависимость скорости выделения ( растворения полония от величины потенциала катода ( кривая диспропорционирования. [16] |
Величины потенциалов, полученные другими авторами [2, 8, 9, 10] для концентрации полония 10 - 8 - 10 - 10 молъ / л, ложатся достаточно близко к нашей экспериментальной прямой; две же точки для концентрации 10 - 13 молъ / л резко отклоняются вверх. [17]
Величина потенциала зависит от ионного фона, однако указанная последовательность комплексов сохраняется как в хлоридпых, так и в сульфатных растворах. [18]
Величина потенциала, необходимого для выделения водорода, меняется вместе с активностью водородных ионов ( эффективная концентрация водородных ионов) в растворе, как это видно из данных табл. 25 ( стр. [19]
Величина потенциала каждого электрода может быть определена сравнением с потенциалом стандартного водородного электрода. Так как окислительно-восстановительные потенциалы, как и электродные потенциалы, зависят от концентрации ионов, участвующих в электродной реакции, то такое сравнение следует проводить при стандартных условиях. [20]
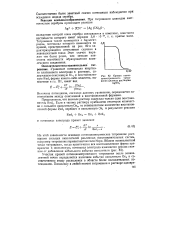 |
Кривая потен-циометрического титрования цианида раствором AgNO3. [21] |
Величина потенциала, согласно данному уравнению, определяется соотношением между окисленной и восстановленной формами. [22]
 |
Капиллярный электрометр [ IMAGE ] Электрокапиллярная кривая. [23] |
Величина потенциала на границе металл - раствор относительно какого-либо электрода сравнения К, например каломельного, измеряется потенциометром, с помощью которого можно накладывать разности потенциала между ртутным мениском и электродом сравнения. При этом потенциал / С остается неизменным, а между электродами проходит ток, доводящий потенциал ртути до желаемой величины. [24]
Величина потенциала этого электрода принимается за нуль. [25]
Величина потенциала, при котором наблюдается перегиб кривой, соответствует началу восстановления ионов и называется потенциалом выделения - Евыд - Его значение зависит от природы восстанавливающихся ионов, их концентрации и других факторов. [26]
Величина потенциала таких электродов определяется концентрацией ионов этих металлов в растворе. Если раствор насыщен труднор. [27]
Величина потенциала таких электродов определяется концентрацией ионов этих металлов в растворе. [28]
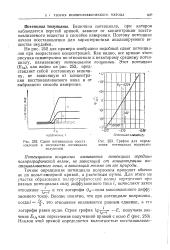 |
Сдвиг потенциалов восстановления и постоянство потенциала полуволны.| График для опреде ления потенциала полуволны. [29] |
Величина потенциала, при котором наблюдается перегиб кривой, зависит от концентрации восстанавливаемого вещества и способов измерения. Поэтому потенциал начала восстановления для характеристики анализируемого вещества неудобен. [30]
Страницы: 1 2 3 4 5