Величина - потенциал
Cтраница 3
Величины потенциалов, отложенных на кривых, соответствуют значениям потенциалов, устанавливающихся в конце катодного и анодного полупериода. Из этих кривых видно, что до тех пор, пока на титане в анодный полу - период происходит активное растворение, потенциал катодной реакции не меняется. При достижении анодного потенциала - 0 3 в наблюдается повышение перенапряжения катодной реакции, несмотря на то, что плотность катодного тока остается постоянной. Это связано с образованием пассивирующего слоя на титане. Таким образом, изменение потенциала катодной реакции при постоянном значении плотности тока в течение катодного полупериода дает возможность зафиксировать потенциал начала пассивации. [32]
Величина потенциала везде отрицательная. [33]
Величины потенциалов вычисляются в милливольтах. [34]
Величина потенциала этого электрода, так же как и других электродов второго рода, может изменяться при комплексообразовании в растворе. Этот эффект рассматривается ниже. [35]
Величина потенциала определяет термодинамическую возможность восстановления того или иного вещества; если потенциал слишком низок, восстановление может не происходить вообще или будут образовываться слабо восстановленные продукты. С повышением потенциала становится возможным образование продуктов более высокой степени восстановления. Так, например, восстановление нитробензола в щелочном растворе на платиновом катоде начинается с заметной скоростью при потенциале около - 0 5 в. В этих условиях главным продуктом является азоксибензол. При потенциале - 1 0 в начинается образование гид разобензола. [36]
Величина потенциала зависит от растворимости металла и от концентрации его ионов в растворе, которые препятствуют растворению. [37]
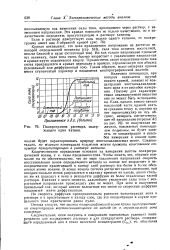 |
Полярограмма раствора, содержащего один катион. [38] |
Величина потенциала, при котором начинается крутой подъем кривой, зависит от концентрации восстанавливливае-мого иона и от способов измерения. Поэтому для характеристики анализируемого вещества она не может быть использована. [39]
Величина потенциала, при котором начинается крутой подъем кривой, зависит от концентрации восстанавливаемого иона и от способов измерения. Поэтому для характеристики анализируемого вещества она не может быть использована. Если, однако, вместо начала наклонной части кривой взять ее среднюю точку и, опустив из нее перпендикуляр на ось абсцисс, измерить соответствующее ей напряжение ( отрезок - АС на рис. 76), то - полученная величина, называемая потенциалом полуволны, не будет зависеть от концентрации и способов измерения и вполне однозначно будет характеризовать природу восстанавливаемых ионов. [40]
Величина потенциала, лионизации может служить мерой большей или меньшей металличности элемента: чем меньше потенциал ионизации, чем легче оторвать электрон от атома, тем сильнее должны быть выражены металлические свойства элемента. [41]
Величина потенциала Ф может быть найдена по вычисленным значениям энтальпии и энтропии. [42]
Величина потенциала на электроде зависит от электрической емкости измерительной системы, интенсивности взаимодействия частиц с электродом и общего электрического поля, определяемого зарядом частиц и размером аппарата. Такие методы измерения предъявляют высокие требования к изоляции измерительной системы, в особенности если регистрируются высокие потенциалы. [43]
Величина потенциала при этом получается приближенной. [44]
Величины потенциалов в вольтах ( или милливольтах) откладываются по оси абсцисс, а соответствующие им величины силы тока в микроамперах-по оси ординат. [45]
Страницы: 1 2 3 4 5
