Величина - потенциал - полуволна
Cтраница 1
Величина потенциала полуволны является вполне определенной характеристикой данной реакции и целиком характеризует природу разряжающихся ионов. [1]
Величина потенциала полуволны, не зависящая ни лт концентрации самого реагирующего вещества, ни от чувствительности гальванометра, ни от скорости вытекания ртути и других факторов, является характеристической константой вещества и в принципе может служить для его качественного определения. Однако качественное исследование раствора полярографическим методом является задачей, в достаточной степени трудной. [2]
Величина потенциала полуволны СС14 в различных смесях органических растворителей и воды зависит от природы индифферентного электролита. [3]
Величина потенциала полуволны определяется главным образом величиной стандартного окислительно-восстановительного потенциала системы, соответствующей электродному процессу ( например, Zn2 / Zn или Fe31f / Fe2), и несколько изменяется с изменением ионной силы раствора. [4]
Величина потенциала полуволны может существенно измениться в том случае, если восстанавливающийся ( окисляющийся) ион образует - комплексное соединение. [5]
Величина потенциала полуволны при восстановлении каждого вида ионов имеет вполне определенное значение. Это позволяет проводить качественный анализ раствора. Высота полярографической волны пропорциональна концентрации восстанавливающегося вещества, поэтому ее измерение служит для количественных определений. [6]
Величины потенциалов полуволн служат для качественной характеристики ионов, имеющихся в растворе. Таким образом, качественный полярографический анализ основан на определении потенциалов полуволн. [7]
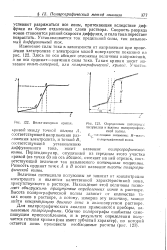 |
Вольт-амперная кривая.| Определение потенциал.. полуволны и высоты полярографической волны. [8] |
Величина потенциала полуволны не зависит от концентрации электролита и является качественной характеристикой иона, присутствующего в растворе. Нахождение этой величины позволяет обнаружить присутствие определенных ионов в растворе. Высота полярографической волны зависит от количества таких ионов в растворе, а потому, измерив эту величину, можно найти концентрацию данного иона в анализируемом растворе. [9]
 |
Графический метод определения потенциала полуволны. [10] |
Величина потенциала полуволны может существенно измениться в том случае, если восстанавливающийся ( или окисляющийся) ион связывается в комплексное соединение. [11]
Величина потенциала полуволны для волны восстановления адсорбированного вещества, как показывает сравнение уравнений ( 1 - 35) и ( 1 - 51 а), зависит не только от константы скорости переноса электронов, но и от адсорбируемости этого вещества. [12]
Величина потенциала полуволны при полярографирова-нии органических соединений обусловлена наличием и природой функциональных групп или заместителей, способных к электроокислению или электровосстановлению. Как правило, потенциал полуволны является полярографической характеристикой органического соединения. Однако под влиянием различных факторов очень часто наблюдается сдвиг потенциала полуволны. [13]
Величина потенциала полуволны при строгом соблюдении постоянных условий электролиза обусловливается наличием и природой функциональных групп или заместителей, способных к электровосстановлению ( или электроокислению) в пределах напряжений, возможных при полярографировании. Пределы напряжений лимитируются природой и свойствами микроэлектрода и фона. Вещества, потенциалы восстановления ( или окисления) которых лежат вне этих пределов, не могут быть определены полярографи-чески на капельном ртутном электроде. Ниже дана краткая полярографическая характеристика наиболее важных классов органических соединений. Рассмотрены только соединения с одноатомными функциями, так как наличие в веществе двух функций или заместителей зачастую сильно меняет полярографическую характеристику вещества. [14]
Величина потенциала полуволны является вполне определенной характеристикой данной реакции и целиком характеризует природу разряжающихся ионов. [15]
Страницы: 1 2 3 4