Величина - потенциал - полуволна
Cтраница 3
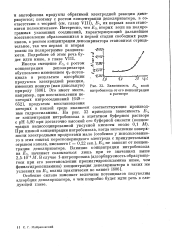 |
Зависимость Е / г волн. [31] |
Особенно сильно изменяет величины потенциалов полуволны адсорбция деполяризатора, о чем подробно будет идти речь в следующей главе. [32]
Предполагаемая Голлом [333] величина потенциала полуволны. [33]
Таким образом, величина потенциала полуволны равна такому значению потенциала рабочего электрода, при котором сила тока равна половине своего предельного значения. [34]
 |
Зависимость Et / волн. [35] |
Особенно сильно изменяет величины потенциалов полуволны адсорбция деполяризатора, о чем подробно будет идти речь в следующей главе. [36]
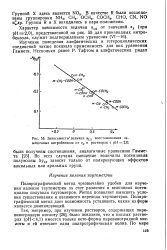 |
Зависимость. величин pj 2 восстановления замещенных нитробензола от sx в растворах с рН 2 0. [37] |
Во всех случаях смещение величины потенциала полуволны Др1 / 2 зависит только от поляризующих эффектов алкильных или арильных групп. [38]
Вообще говоря, в величину потенциала полуволны следует включить еще и отношение АО / ИВ [ в ур. Штрелову и Штакель-бергу 148, очень мало зависит от периода капания и веса капли. Однако наиболее существенными величинами для определения потенциала полуволны являются стандартный потенциал Е0 металла ( для Ме / Мег) и коэффициент активности металла ув в амальгаме. [40]
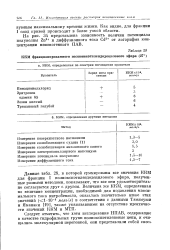 |
ККМ фракционированного полиоксиэтплендодецплового эфира ( 27. [41] |
На рис. 34 представлена зависимость величин потенциала полуволны Zn2 и диффузионного тока Cd2 от логарифма концентрации неионогенного ПАВ. [42]
В табл. 19 приведены значения величин потенциалов полуволн наиболее часто встречающихся ненасыщенных органических кислот. [43]
Интересно отметить, что по величине потенциала полуволны одноэлектронного восстановления ТЦНЭ несколько более сильный акцептор, чем ТЦНХ, так как в отличие от метода, основывающегося на сравнении констант комплексообразования, при определении силы акцептора по полярографическим данным элиминируются такие факторы, как пространственные затруднения координации и относительные размеры молекул. [44]
Из приведенных уравнений видно, что величины потенциалов полуволн восстановления нитробензола должны сильно зависеть от концентрации водородных ионов, так как они участвуют в реакциях восстановления. В буферных растворах при рН 2 первая волна восстановления наблюдается при потенциале - 0 15 в, в нейтральных растворах ( рН 7) - при - 0 47 в, а в щелочных растворах - при - 0 63 в. [45]
Страницы: 1 2 3 4