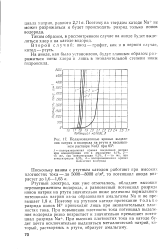
Величина - нормальный потенциал
Cтраница 3
В связи со всем сказанным представляло известный интерес и то сопоставление величин нормальных потенциалов металлов с типом их кристаллической решетки, которое было нами своевременно изложено [3] и которое показало наличие здесь определенной закономерной связи. [31]
Величины вычисленных выше окислительно-восстановительных потенциалов, как мы видим, мало отличаются от величин нормальных потенциалов. Это дает возможность во многих случаях, если величины EQ значительно разнятся между собой, для решения вопроса о направлении реакции сопоставлять только нормальные потенциалы. [32]
Однако этих двух примеров недостаточно, чтобы считать возможным правильно вычислять таким способом величины абсолютных и нормальных потенциалов. Следует также учесть, что точности результатов может сильно повредить ненадежность исходных физических величин. [33]
С целью определить, свободны ли полиметиленовые кольца от напряжения, полученные значения сравнили с величиной нормального потенциала окислительно-восстановительной системы 2 6-диэтилгидрохинон - 2 6-диэтилбензохинон. Полученные данные позволили заключить, что изученные системы являются обратимыми. [34]
В то же время для двух окислительно-восстановительных систем Fe3 / Fe2 и J2 / J - величины нормальных потенциалов весьма близки: 0 77 и 0 54 в, их разность составляет всего 0 23 в, однако процесс окисления ионов иода попами трехвалентного железа протекает довольно легко. [35]
Подобного же рода ориентировочные оценки могут быть сделаны для комбинаций разных металлов с разными анионами, для которых известны величины нормальных потенциалов. [36]
 |
Ряд окислительных потенциалов некоторых систем. [37] |
В тех случаях, когда в реакциях принимают участие водородные ( гидро-ксильные) ионы, указанные на рис. 85 величины нормальных потенциалов относятся к 1 М концентрации этих ионов. [38]
Выше указывалось, что в некоторых случаях окислительно-восстановительные реакции протекают крайне медленно, поэтому определение возможности таких реакций по величине нормальных потенциалов оказывается практически бесполезным, так как при этом не достигаются равновесные значения потенциалов. Согласно закону действующих масс, скорость реакции оказывается небольшой в том случае, когда концентрация одного из веществ слишком мала. Но часто и при больших концентрациях один из двух процессов - окисление или восстановление - протекает так медленно, что равновесие не может установиться в продолжение большого отрезка времени. [39]
Выше указывалось, что в некоторых случаях окислительно-восстановительные реакции протекают крайне медленно, поэтому определение возможности таких реакций по величине нормальных потенциалов оказывается практически бесполезным, так как при этом не достигаются равновесные значения потенциалов. Согласно закону действующих масс, скорость реакции оказывается небольшой в том случае, когда концентрация одного из веществ слишком мала. Но часто и при больших концентрациях один из двух процессов - окисление или восстановление - протекает так медленно, что равновесие не может установиться в продолжение большого отрезка времени. [40]
Выше указывалось, что в некоторых случаях окислительно-восстановительные реакции протекают крайне медленно, поэтому определение возможности таких реакций по величине нормальных потенциалов оказывается практически бесполезным, так как при этом не достигаются равновесные значения потенциалов. Согласно закону действующих масс, скорость реакции оказывается небольшой в том случае, когда концентрация одного из веществ слишком мала. Но часто и при больших концентрациях один из двух процессов - окисление или восстановление - протекает так медленно, что равновесие не может установиться в продолжение большого отрезка времени. [41]
Окислительно-восстановительный потенциал в целом, в соответствии с формулой ( 40), зависит, с одной стороны, от величины нормального потенциала, с другой - от отношения концентраций окисленной и восстановленной форм. [42]
В каких случаях сравнительная активность металлов может оцениваться по величинам ионизационных потенциалов их атомов и в каких случаях - по величинам нормальных потенциалов металлов. [43]
Ртутный электрод, как уже отмечалось, обладает высоким перенапряжением водорода, а равновесный потенциал разряда ионов натрия на ртути значительно ниже величины нормального потенциала натрия из-за образования амальгамы Na и не превышает 1 8 в. Поэтому на ртутном катоде протекание только разряда ионов Н происходит лишь при незначительных плотностях тока. При высоких плотностях тока на катоде будет почти исключительно выделяться металлический натрий, который, растворяясь в ртути, образует амальгаму. [45]
Страницы: 1 2 3 4